ХАЙРІМОЗ
-
Австрія Сандоз ГмбХФорма выпуска: розчин для ін'єкцій, 100 мг/мл, по 40 мг/0,4 мл або по 20 мг/0,2 мл розчину в попередньо наповненому шприці; по 2 попередньо наповнених шприців у блістерах у картонній коробціСостав: 1 попередньо наповнений шприц містить 20 мг адалімумабу у 0,2 мл розчину;/1 попередньо наповнений шприц містить 40 мг адалімумабу у 0,4 мл розчинуУсловия отпуска: за рецептомНомер регистрационного свидетельства: UA/21181/01/02код АТХ: L04AB04Срок годности: 2 роки.
-
Австрія Сандоз ГмбХФорма выпуска: розчин для ін'єкцій, 50 мг/мл, по 40 мг/0,8 мл розчину в попередньо наповненому шприці; по 2 попередньо наповнених шприців у блістерах у картонній коробціСостав: 1 попередньо наповнений шприц містить 40 мг адалімумабу у 0,8 мл розчинуУсловия отпуска: за рецептомНомер регистрационного свидетельства: UA/21181/01/01код АТХ: L04AB04Срок годности: 30 місяців.
ІНСТРУКЦІЯ
для медичного застосування лікарського засобу
Хайрімоз
(Hyrimoz)
Склад:
діюча речовина: адалімумаб;
1 попередньо наповнений шприц містить 20 мг адалімумабу у 0,2 мл розчину;
допоміжні речовини: кислота адипінова; маніт (Е 421); полісорбат 80; натрію гідроксид (для коригування рН); кислота хлористоводнева (для коригування рН); вода для ін’єкцій.
Лікарська форма. Розчин для ін’єкцій.
Основні фізико-хімічні властивості: прозорий або дещо опалесцюючий, безбарвний або злегка жовтуватий розчин.
Фармакотерапевтична група.
Імуносупресанти. Інгібітори фактора некрозу пухлини-альфа. Адалімумаб.
Код АТХ L04А В04.
Фармакологічні властивості
Механізм дії
Адалімумаб специфічно зв’язується з фактором некрозу пухлин (ФНП) та нейтралізує біологічні ефекти ФНП, блокуючи його взаємодію з p55- та p75-рецепторами ФНП на поверхні клітини.
Адалімумаб модулює також біологічні реакції відповіді, що індукуються або регулюються ФНП, включаючи зміни рівнів молекул адгезії, відповідальних за міграцію лейкоцитів (ELAM-1, VCAM-1 та ICAM-1 при IC50 0,1–0,2 нМ).
Фармакодинаміка
У пацієнтів з ревматоїдним артритом (РА) адалімумаб спричиняв швидке зменшення, порівняно з початковими параметрами, рівнів показників гострої фази запалення (С-реактивного протеїну (СРП), цитокінів сироватки крові (IL-6) та швидкості осідання еритроцитів (ШОЕ)) у пацієнтів з ревматоїдним артритом. Також спостерігалося зниження рівнів матриксних металопротеїназ (MMP-1 та MMP-3) у сироватці крові, які спричиняють ремоделювання тканин, що лежить в основі руйнування хряща. При застосуванні адалімумабу зазвичай спостерігається покращення гематологічних ознак хронічного запалення.
Після лікування адалімумабом швидке зниження рівнів СРП спостерігалося також і у пацієнтів з поліартикулярним ювенільним ідіопатичним артритом (ЮІА), хворобою Крона (ХК), виразковим колітом (ВК) та гнійним гідраденітом (ГГ). Водночас зі значущим зменшенням експресії ФНП-α у пацієнтів з хворобою Крона спостерігалося зменшення кількості клітин, що експресують запальні маркери в товстій кишці. Ендоскопічні дослідження слизової оболонки кишечнику пацієнтів, які отримували адалімумаб, продемонстрували ознаки загоєння.
Фармакокінетика
Абсорбція та розподіл
Після одноразового підшкірного введення 40 мг адалімумабу абсорбція та розподіл адалімумабу були повільними, середня пікова концентрація в сироватці крові досягалася приблизно через 5 днів після введення. Середня абсолютна біодоступність адалімумабу, розрахована в трьох дослідженнях, після застосування одноразової дози 40 мг підшкірно становила 64 %.
Після одноразового внутрішньовенного введення у дозах від 0,25 до 10 мг/кг концентрації були пропорційні дозам. Після застосування дози 0,5 мг/кг (приблизно 40 мг) кліренс був у діапазоні 11–15 мл/год, об’єм розподілу (Vss) становив від 5 до 6 л, середній термінальний період напіввиведення становив приблизно 2 тижні. Концентрації адалімумабу у синовіальній рідині у пацієнтів з РА становили 31–96 % від рівня в сироватці крові.
Після підшкірного застосування адалімумабу у дозі 40 мг 1 раз на 2 тижні у пацієнтів з РА рівноважні концентрації становили від 5 мкг/мл (без супутнього застосування метотрексату) до 8–9 мкг/мл (з метотрексатом) відповідно. Концентрації адалімумабу в сироватці крові у рівноважному стані зростали майже пропорційно до підшкірно введених доз 20, 40 та 80 мг 1 раз на 2 тижні або щотижня.
Після підшкірного застосування адалімумабу у дозі 24 мг/м2 (до 40 мг) 1 раз на 2 тижні у пацієнтів з поліартикулярним ювенільним ревматоїдним артритом (ЮРА) віком від 4 до 17 років рівноважні концентрації (показники вимірювались з 20-го по 48-й тиждень) становили 5,6 ± 5,6 мкг/мл (102 % CV – коефіцієнт варіації) без супутнього застосування метотрексату та 10,9 ± 5,2 мкг/мл (47,7 % CV) – з метотрексатом.
У дітей з поліартикулярним ЮРА віком 2–4 роки та у дітей віком від 4 років, маса тіла яких менше 15 кг, після застосування адалімумабу у дозі 24 мг/м2 з метотрексатом середнє значення рівноважних концентрацій становило 6,0 ± 6,1 мкг/мл (101 % CV) без супутнього застосування метотрексату та 7,9 ± 5,6 мкг/мл (71,2 % CV) – з метотрексатом.
Після підшкірного застосування адалімумабу у дозі 24 мг/м2 (до 40 мг) 1 раз на 2 тижні у пацієнтів віком від 6 до 17 років з ентезитасоційованим артритом рівноважні концентрації (показники вимірювались на 24-му тижні) становили 8,8 ± 6,6 мкг/мл без супутнього застосування метотрексату та 11,8 ± 4,3 мкг/мл – з метотрексатом.
Після підшкірного застосування адалімумабу в дозі 40 мг 1 раз на 2 тижні дорослим пацієнтам з нерентгенологічним аксіальним спондилоартритом середня (± стандартне відхилення) рівноважна концентрація на тижні 68 становила 8,0 ± 4,6 мкг/мл.
У дорослих пацієнтів із псоріазом середня рівноважна концентрація становила 5 мкг/мл протягом монотерапії адалімумабом у дозі 40 мг 1 раз на 2 тижні.
Після підшкірного застосування адалімумабу у дозі 0,8 мг/кг (до максимум 40 мг) 1 раз на 2 тижні у дітей із хронічним бляшковим псоріазом рівноважні концентрації становили приблизно 7,4 ± 5,8 мкг/мл (79 % CV).
У пацієнтів з гнійним гідраденітом після введення адалімумабу у дозі 160 мг на тижні 0 з наступним введенням 80 мг на тижні 2 його концентрація у сироватці крові становила приблизно від 7 до 8 мкг/мл на тижні 2 та тижні 4. Середня рівноважна концентрація з тижня 12 до тижня 36 становила приблизно від 8 до 10 мкг/мл під час введення адалімумабу у дозі 40 мг кожного тижня.
Вплив адалімумабу на підлітків з гідраденітом було визначено за допомогою фармакокінетичного моделювання та симуляції на основі фармакокінетики при інших показаннях у дітей (бляшковий псоріаз, ювенільний ревматоїдний (ідіопатичний) артрит (ЮРА), хвороба Крона (ХК) та ентезитасоційований артрит). Рекомендований режим дозування для підлітків з гідраденітом – 40 мг 1 раз на 2 тижні. Оскільки вплив адалімумабу може залежати від маси тіла, підліткам з високою масою тіла та недостатньою відповіддю на лікування можна застосовувати рекомендовану дозу для дорослих – по 40 мг 1 раз на тиждень.
У пацієнтів з хворобою Крона після введення адалімумабу у дозі 80 мг на тижні 0 з наступним введенням 40 мг на тижні 2 концентрація у сироватці крові становила приблизно 5,5 мкг/мл протягом індукційної терапії. Після введення адалімумабу у дозі 160 мг на тижні 0 з наступним введенням 80 мг на тижні 2 його концентрація у сироватці крові становила приблизно 12 мкг/мл протягом індукційної терапії. Середня рівноважна концентрація становила приблизно 7 мкг/мл під час введення адалімумабу у підтримуючій дозі 40 мг 1 раз на 2 тижні.
У дітей з хворобою Крона середнього та високого ступеня активності початкова доза адалімумабу у відкритому дослідженні становила 160/80 мг або 80/40 мг на тижнях 0 та 2 залежно від маси тіла. На тижні 4 пацієнти були рандомізовані в співвідношенні 1 : 1 у групи, які отримували залежно від маси тіла або стандартну дозу (40/20 мг 1 раз на 2 тижні), або низьку дозу (20/10 мг 1 раз на 2 тижні) для підтримуючої терапії. Середня рівноважна концентрація становила приблизно 15,7 ± 6,6 мкг/мл на тижні 4 у пацієнтів з масою тіла 40 кг або більше (160/80 мг) та 10,6 ± 6,1 мкг/мл у пацієнтів з масою тіла менше 40 кг (80/40 кг).
У пацієнтів, які продовжували лікування в своїй групі, середні (± стандартне відхилення) концентрації адалімумабу на тижні 52 становили 9,5 ± 5,6 мкг/мл у групі стандартних доз та 3,5 ± 2,2 мкг/мл у групі низьких доз. Середні концентрації зберігалися у пацієнтів, які продовжували отримувати лікування адалімумабом протягом 52 тижнів. Для пацієнтів, яким дозу збільшили з однієї 1 раз на два тижні до однієї щотижня, середні (± стандартне відхилення) концентрації адалімумабу в сироватці крові на тижні 52 становили 15,3 ± 11,4 мкг/мл (40/20 мг, щотижня) та 6,7 ± 3,5 мкг/мл (20/10 мг, щотижня).
У пацієнтів з виразковим колітом після введення адалімумабу у початковій дозі 160 мг на тижні 0 з наступним введенням 80 мг на тижні 2 його концентрація у сироватці крові становила приблизно 12 мкг/мл протягом індукційної терапії. Середня рівноважна концентрація становила приблизно 8 мкг/мл під час введення адалімумабу у підтримуючій дозі 40 мг 1 раз на 2 тижні.
У дітей з виразковим колітом середня рівноважна концентрація адалімумабу у сироватці крові на тижні 52 після підшкірного введення дози залежно від маси тіла 0,6 мг/кг (максимум 40 мг) один раз на два тижні становила 5,01 ± 3,28 мкг/мл. У пацієнтів, яким вводили дозу 0,6 мг/кг (максимум 40 мг) кожного тижня, середня (± стандартне відхилення) рівноважна концентрація адалімумабу в сироватці крові на тижні 52 становила 15,7 ± 5,60 мкг/мл.
У дорослих пацієнтів з увеїтом після введення адалімумабу у початковій дозі 80 мг на тижні 0 з наступним введенням 40 мг 1 раз на 2 тижні, починаючи з тижня 1, середня рівноважна концентрація становила приблизно від 8 до 10 мкг/мл.
Вплив адалімумабу на стан дітей з увеїтом було визначено за допомогою фармакокінетичного моделювання та симуляції на основі фармакокінетики при інших показаннях у дітей (бляшковий псоріаз, ювенільний ревматоїдний (ідіопатичний) артрит (ЮРА), хвороба Крона (ХК) та ентезитасоційований артрит). Немає клінічних даних про вплив початкової дози адалімумабу на стан дітей віком до 6 років. Прогнозується, що за відсутності метотрексату початкова доза може призвести до підвищення системного впливу.
Популяційне фармакокінетичне та фармакокінетичне/фармакодинамічне моделювання і симуляція передбачили порівнянний вплив та ефективність адалімумабу в пацієнтів, які отримували 80 мг 1 раз на 2 тижні, та у пацієнтів, які отримували щотижнево дозу 40 мг (включаючи дорослих пацієнтів з РА, ГГ, ВК, ХК або псоріазом, дітей з ГГ та дітей масою тіла 40 кг і більше з ХК та ВК).
Залежність «вплив – відповідь» у дітей
На основі даних клінічних досліджень у пацієнтів з ЮІА (поліартикулярний ювенільний ідіопатичний артрит та ентезитасоційований артрит) було встановлено залежність «вплив – відповідь» між концентрацією в плазмі крові та відповіддю за критерієм PedACR 50. Очевидна концентрація адалімумабу в плазмі крові, яка забезпечує половину максимальної ймовірності відповіді PedACR 50 (EC50), становила 3 мкг/мл (95 % ДІ 1–6 мкг/мл). Залежність «вплив – відповідь» між концентрацією адалімумабу та його ефективністю у дітей з хронічним бляшковим псоріазом високого ступеня тяжкості була встановлена для відповідей за індексом PASI 75 та PGA («відсутність» або «мінімальний» відповідно). Показники PASI 75 та PGA «відсутність» або «мінімальний» зростали зі збільшенням концентрації адалімумабу, при цьому обидва показники мали подібну явну EC50 приблизно 4,5 мкг/мл (95 % ДІ 0,4–47,6 та 1,9–10,5 відповідно).
Виведення
Популяційний фармакокінетичний аналіз даних більше ніж 1300 пацієнтів з РА виявив тенденцію до підвищення явного кліренсу адалімумабу з підвищенням маси тіла пацієнтів. З урахуванням поправок щодо різниці маси тіла було встановлено, що стать та вік пацієнта мають мінімальний вплив на кліренс адалімумабу. Рівні вільного адалімумабу (не зв’язаного з антитілами до адалімумабу в сироватці крові були нижчими у пацієнтів, у яких виявлялись антитіла до адалімумабу. Не вивчали застосування лікарського засобу Хайрімоз пацієнтам із порушеннями функцій печінки та нирок.
Клінічні характеристики
Показання
Ревматоїдний артрит (РА)
Хайрімоз у комбінації з метотрексатом показаний для:
· лікування ревматоїдного артриту середнього та високого ступеня активності у дорослих пацієнтів, коли адекватна відповідь на терапію протиревматичними препаратами, що модифікують перебіг захворювання (DMARDs – disease-modifying antirheumatic drugs), включаючи метотрексат, не була отримана;
· лікування активного прогресуючого ревматоїдного артриту високого ступеня активності у дорослих пацієнтів, які раніше не отримували терапію метотрексатом.
Хайрімоз можна застосовувати як монотерапію у разі непереносимості метотрексату або коли продовження терапії метотрексатом є неприйнятним.
Адалімумаб продемонстрував пригнічення прогресування структурного ураження суглобів, що було підтверджено рентгенографічно, та покращення функціонального стану при одночасному застосуванні з метотрексатом.
Ювенільний ревматоїдний (ідіопатичний) артрит (ЮРА)
Поліартикулярний ювенільний ревматоїдний (ідіопатичний) артрит
Хайрімоз у комбінації з метотрексатом показаний для лікування активного поліартикулярного ювенільного ідіопатичного артриту у дітей віком від 2 років, у яких не було адекватної відповіді на терапію одним або кількома протиревматичними препаратами, що модифікують перебіг захворювання (DMARDs).
Хайрімоз можна застосовувати як монотерапію у разі непереносимості метотрексату або коли продовження терапії метотрексатом є неприйнятним. Не було проведено досліджень застосування препарату Хайрімоз пацієнтам віком до 2 років.
Ентезитасоційований артрит
Хайрімоз показаний для лікування активного ентезитасоційованого артриту у дітей віком від 6 років, які не відповідали на традиційну терапію або мають непереносимість чи медичні протипоказання до таких видів терапії.
Аксіальний спондилоартрит
Анкілозуючий спондиліт (АС)
Хайрімоз показаний для лікування анкілозуючого спондиліту з високим ступенем активності у дорослих пацієнтів, які не відповіли на традиційну терапію.
Аксіальний спондилоартрит без рентгенологічного підтвердження АС
Хайрімоз показаний для лікування аксіального спондилоартриту з високим ступенем активності без рентгенологічного підтвердження АС, але з наявними ознаками запалення на підставі підвищеного рівня СРП та/або за результатами МРТ (магнітно-резонансна томографія) у дорослих пацієнтів, у яких не було адекватної відповіді на терапію нестероїдними протизапальними препаратами (НПЗП) або наявна непереносимість цих препаратів.
Псоріатичний артрит (ПсА)
Хайрімоз показаний для лікування активного та прогресуючого псоріатичного артриту у дорослих пацієнтів, коли не було отримано адекватної відповіді на попередню терапію протиревматичними препаратами, що модифікують перебіг захворювання (DMARDs). Адалімумаб продемонстрував уповільнення темпів прогресування ураження периферичних суглобів, що визначається за допомогою рентгенографії, у пацієнтів із симетричною поліартикулярною формою захворювання та покращання функціонального стану.
Бляшковий псоріаз (БП)
Хайрімоз показаний для лікування дорослих пацієнтів із помірним або тяжким перебігом хронічного бляшкового псоріазу, яким необхідна системна терапія.
Бляшковий псоріаз (БП) у дітей
Хайрімоз показаний для лікування хронічного бляшкового псоріазу з тяжким перебігом у дітей віком від 4 років, у яких не отримано клінічної відповіді або є протипоказання/ непереносимість місцевої терапії або фототерапії.
Гнійний гідраденіт (ГГ)
Хайрімоз показаний для лікування активного помірного та тяжкого гнійного гідраденіту (acne inversa) у дорослих пацієнтів та у підлітків віком від 12 років, які не відповідали на традиційну системну терапію.
Хвороба Крона (ХК)
Хайрімоз показаний для лікування хвороби Крона середнього та високого ступеня активності у дорослих пацієнтів, які не відповідали на повний курс терапії кортикостероїдами та/або імуносупресантами або мають непереносимість чи медичні протипоказання до таких видів терапії.
Хвороба Крона (ХК) у дітей
Хайрімоз показаний для лікування хвороби Крона середнього та високого ступеня активності у дітей віком від 6 років, які не відповідали на традиційну терапію, включаючи первинну нутритивну терапію, терапію кортикостероїдами та/або імуномодуляторами, або мають непереносимість чи медичні протипоказання до таких видів терапії.
Виразковий коліт (ВК)
Хайрімоз показаний для лікування виразкового коліту середнього та високого ступеня активності у дорослих, які не відповідали на традиційну терапію, включаючи терапію кортикостероїдами та/або 6-меркаптопурином або азатіоприном, або мають непереносимість чи медичні протипоказання до таких видів терапії.
Виразковий коліт (ВК) у дітей
Хайрімоз показаний для лікування виразкового коліту середнього та високого ступеня активності у дітей (віком від 6 років), які не відповідали на традиційну терапію, включаючи терапію кортикостероїдами та/або 6-меркаптопурином або азатіоприном, або мають непереносимість чи медичні протипоказання до таких видів терапії.
Увеїт
Хайрімоз показаний для лікування неінфекційного інтермедіарного, заднього та панувеїту у дорослих пацієнтів, які не відповідали на терапію кортикостероїдами, яким необхідно знизити дозу кортикостероїдів або які мають непереносимість чи медичні протипоказання до терапії кортикостероїдами.
Увеїт у дітей
Хайрімоз показаний для лікування хронічного неінфекційного переднього увеїту у дітей віком від 2 років, які не відповідали на традиційну терапію або мають непереносимість традиційної терапії або яким традиційна терапія протипоказана.
Протипоказання
· Підвищена чутливість до адалімумабу або до будь-якого іншого компонента препарату.
· Активний туберкульоз або інші тяжкі інфекції, такі як сепсис та опортуністичні інфекції (див. розділ «Особливості застосування»).
· Помірна та тяжка серцева недостатність (III/IV клас за NYHA) (див. розділ «Особливості застосування»).
Взаємодія з іншими лікарськими засобами та інші види взаємодій
Адалімумаб вивчали за участю пацієнтів з РА, ЮРА та ПсА, які отримували препарат як монотерапію та одночасно з метотрексатом. Рівень формування антитіл був нижчим при одночасному застосуванні адалімумабу з метотрексатом порівняно з монотерапією. Введення адалімумабу без метотрексату призводило до збільшення рівня формування антитіл, збільшення кліренсу та зниження ефективності адалімумабу.
· Не рекомендується одночасне застосовування препарату Хайрімоз із анакінрою (див. розділ «Особливості застосування»).
· Не рекомендується одночасне застосовування препарату Хайрімоз із абатацептом (див. розділ «Особливості застосування»).
Особливості застосування.
З метою покращення контролю застосування біологічних препаратів необхідно чітко фіксувати торгівельну назву та номер серії введеного препарату у медичній документації пацієнта.
Інфекції
Пацієнти, які застосовували блокатори ФНП, більш схильні до розвитку тяжких інфекцій.
Порушення функції легенів може збільшити ризик розвитку інфекцій. Тому за станом пацієнтів слід ретельно стежити та перевіряти на наявність інфекцій, включаючи туберкульоз, до, під час та після лікування препаратом Хайрімоз. Оскільки елімінація адалімумабу може тривати до чотирьох місяців, спостереження слід продовжувати протягом цього періоду.
Не слід застосовувати адалімумаб пацієнтам з активним інфекційним процесом, включаючи хронічні або локалізовані інфекції, поки інфекція не буде контрольована. У пацієнтів, які мають контакт із хворим на туберкульоз або повернулися з країн з високим рівнем захворюваності на туберкульоз або з ендемічних зон щодо мікозів (гістоплазмоз, кокцидіоїдомікоз або бластомікоз), слід оцінити співвідношення користь/ризик до початку застосування препарату Хайрімоз (див. нижче «Інші опортуністичні інфекції»).
Необхідно провести повне обстеження та ретельно спостерігати за станом пацієнтів, у яких під час лікування препаратом Хайрімоз розвинулася нова інфекція. При розвитку тяжкої інфекції або сепсису слід припинити лікування та застосувати відповідні протимікробні або протигрибкові препарати, поки інфекція не буде контрольована. Слід з особливою обережністю застосовувати Хайрімоз пацієнтам з рекурентними інфекціями або при преморбідних станах, що підвищують схильність до розвитку інфекцій.
Тяжкі інфекції
Тяжкі інфекції, такі як сепсис, спричинений бактеріальними, мікобактеріальними, інвазивними грибковими, паразитарними, вірусними або іншими опортуністичними інфекціями (лістеріоз, легіонельоз і пневмоцистоз), спостерігалися у пацієнтів, які застосовували адалімумаб.
У клінічних дослідженнях спостерігалися й інші тяжкі інфекції: пневмонія, пієлонефрит, септичний артрит та септицемія. Були повідомлення про госпіталізацію пацієнтів з інфекціями, що виникли (у тому числі про летальні випадки).
Туберкульоз
Повідомлялося про випадки реактивації та про розвиток нової інфекції туберкульозу, включаючи легеневу та нелегеневу форми (тобто дисемінований туберкульоз), у пацієнтів, які отримували лікування адалімумабом. До початку терапії препаратом Хайрімоз пацієнтів потрібно ретельно обстежити щодо активного та неактивного (латентного) туберкульозу. Обстеження повинно включати вичерпну оцінку анамнезу пацієнта з туберкульозом або відомості про можливі контакти з хворими на активний туберкульоз та про попередню та/або супутню імуносупресивну терапію. Слід провести всім пацієнтам до початку терапії шкірний туберкуліновий тест (проба Манту) та рентгенографію грудної клітки (можуть застосовуватися місцеві рекомендації). Проведення та результати проб рекомендується фіксувати в картці-пам’ятці пацієнта. Лікарі повинні пам’ятати про ризик хибнонегативних результатів шкірних туберкулінових тестів, особливо у тяжкохворих пацієнтів або пацієнтів з ослабленим імунітетом.
Терапію лікарським засобом Хайрімоз не слід проводити, якщо діагностується активний туберкульоз (див. розділ «Протипоказання»).
У всіх ситуаціях, описаних нижче, слід дуже ретельно зважити співвідношення користь/ризик терапії.
Рішення про лікування пацієнтів з підозрою на латентний туберкульоз слід приймати після консультації з фтизіатром.
У разі латентного туберкульозу перед початком терапії лікарським засобом Хайрімоз потрібно провести специфічне протитуберкульозне лікування відповідно до місцевих рекомендацій.
Слід зважати на необхідність протитуберкульозного лікування перед початком терапії лікарським засобом Хайрімоз пацієнтам, які мають фактори ризику розвитку туберкульозної інфекції, але в яких отримано негативний результат тесту на латентний туберкульоз, та пацієнтам, які мали в анамнезі латентний або активний туберкульоз і для яких не може бути підтверджене відповідне лікування.
Незважаючи на профілактичне протитуберкульозне лікування, випадки реактивації туберкульозу траплялися у пацієнтів, які отримували адалімумаб. У деяких пацієнтів, які раніше перенесли успішну терапію активного туберкульозу, спостерігався повторний розвиток туберкульозу на тлі прийому адалімумабу.
Усіх пацієнтів потрібно попередити про необхідність консультації лікаря у разі появи ознак, що нагадують симптоми туберкульозу (наприклад, постійний кашель, виснаження / зменшення маси тіла, субфебрильна температура, апатія) під час або після лікування препаратом Хайрімоз.
Інші опортуністичні інфекції
Протягом лікування адалімумабом повідомлялося про розвиток опортуністичних інфекцій, у тому числі інвазивних грибкових інфекцій. Іноді такі інфекції своєчасно не діагностувалися у пацієнтів, які застосовують антагоністи ФНП, що призводило до пізнього початку лікування та іноді завершувалося летально.
У разі розвитку лихоманки, нездужання, зменшення маси тіла, підвищення пітливості, кашлю, задишки та/або інфільтратів у легенях чи інших ознак серйозного системного захворювання (з шоком або без) пацієнтам слід негайно пройти обстеження щодо виявлення інвазивної грибкової інфекції та негайно припинити застосування препарату Хайрімоз. Рішення щодо застосування емпіричної протигрибкової терапії таким хворим слід приймати після консультації з фахівцем у сфері діагностики та лікування інвазивних грибкових інфекцій.
Реактивація гепатиту В.
Застосування блокаторів ФНП, включаючи адалімумаб, пов’язувалося з реактивацією вірусу гепатиту В у хронічних носіїв (тобто тих, хто мав позитивний поверхневий антиген). Іноді випадки реактивації вірусу гепатиту В були летальними. До початку застосування препарату Хайрімоз слід обстежити пацієнтів групи ризику щодо вірусу гепатиту В. У разі позитивного результату такого обстеження рішення про лікування слід приймати після консультації з гепатологом.
Слід з обережністю призначати Хайрімоз пацієнтам, які є носіями вірусу гепатиту В, а у разі призначення – ретельно спостерігати за станом таких пацієнтів щодо появи симптомів реактивації вірусу гепатиту В під час терапії та протягом декількох місяців після припинення лікування. Немає даних щодо ефективності та безпеки застосування противірусних препаратів для профілактики реактивації вірусу гепатиту В у носіїв, які отримують антагоністи ФНП для запобігання реактивації вірусу гепатиту В. При реактивації вірусу гепатиту В слід припинити терапію препаратом Хайрімоз й призначити ефективне противірусне лікування та відповідну підтримуючу терапію.
Неврологічні розлади
При застосуванні блокаторів ФНП, у тому числі адалімумабу, повідомлялося про поодинокі випадки появи або загострення клінічних симптомів та/або радіографічних ознак демієлінізуючих захворювань центральної нервової системи, включаючи розсіяний склероз, неврит зорового нерва та демієлінізуючі захворювання периферичної нервової системи, включаючи синдром Гійєна – Барре. Рекомендується ретельна оцінка переваг/ризику застосування адалімумаба для пацієнтів з демієлінізуючими розладами центральної або периферичної нервової системи. Необхідно припинити терапію препаратом Хайрімоз у разі виникнення зазначених розладів. Відомо, що існує зв’язок між інтермедіарним увеїтом та демієлінізуючими розладами центральної нервової системи. Неврологічне обстеження необхідно проводити пацієнтам з неінфекційним інтермедіарним увеїтом перед тим, як розпочати терапію лікарським засобом Хайрімоз, та регулярно протягом терапії, щоб оцінювати розвиток демієлінізуючих розладів центральної нервової системи.
Алергічні реакції
Під час клінічних досліджень виникали поодинокі серйозні алергічні реакції, пов’язані з адалімумабом. Повідомлялося про серйозні алергічні реакції, включаючи анафілаксію, після введення адалімумабу. При виникненні анафілактичної реакції або іншої серйозної алергічної реакції необхідно негайно припинити застосування препарату Хайрімоз і розпочати відповідну терапію.
Імуносупресія
Під час клінічних досліджень адалімумабу у 64 пацієнтів з РА випадків пригнічення гіперчутливості сповільненого типу, зниження рівнів імуноглобулінів або кількісних змін ефекторних Т- та В-клітин, а також NK-клітин, моноцитів/макрофагів та нейтрофілів не спостерігалося.
Злоякісні новоутворення
У контрольованих клінічних дослідженнях блокаторів ФНП частіше повідомлялося про розвиток злоякісних новоутворень у пацієнтів, які отримували ФНП-блокатор, ніж у пацієнтів контрольної групи. Однак ці випадки були поодинокими. У постмаркетинговій практиці повідомлялося про випадки лейкемії, пов’язаної із застосуванням антагоністів ФНП. Більше того, у пацієнтів з давнім високоактивним ревматоїдним артритом існує високий фоновий ризик виникнення лімфоми та лейкемії, що ускладнює оцінку ризику. З огляду на існуючі дані не можна виключати ризик розвитку лімфом, лейкемії або інших злоякісних новоутворень у пацієнтів, які лікуються антагоністами ФНП.
З постмаркетингової практики відомо про випадки злоякісних новоутворень (у тому числі летальних) у дітей та дорослих (віком до 22 років), які отримували лікування антагоністами ФНП (вік початку терапії ≤ 18 років), включаючи адалімумаб. Лімфоми становили приблизно половину цих випадків. Решту становили різні злоякісні новоутворення, в тому числі рідкісні злоякісні новоутворення, що зазвичай асоціюються з імуносупресією. Не можна виключити ризик розвитку злоякісних новоутворень у дітей, які отримують лікування антагоністами ФНП.
У постмаркетинговій практиці були поодинокі повідомлення про розвиток гепатолієнальної Т-клітинної лімфоми у пацієнтів, які застосовували адалімумаб. Це рідкісний тип лімфоми, що характеризується дуже агресивним перебігом та зазвичай є летальним. Деякі випадки утворення гепатолієнальної Т-клітинної лімфоми на тлі лікування адалімумабом спостерігалися в молодих людей, які раніше отримували терапію інфліксимабом у комбінації з азатіоприном або 6-меркаптопурином для лікування запальних захворювань кишечнику. Потенційний ризик одночасного застосування азатіоприну або 6-меркаптопурину з адалімумабом має бути ретельно оцінений. Ризик розвитку гепатолієнальної Т-клітинної лімфоми у пацієнтів, які отримують лікування препаратом Хайрімоз, виключити не можна (див. розділ «Побічні реакції»).
Досліджень щодо застосування адалімумабу пацієнтам зі злоякісними новоутвореннями в анамнезі або продовження терапії у пацієнтів, в яких розвинулося злоякісне новоутворення, не проводилося. Отже, це потрібно враховувати та з обережністю приймати рішення щодо застосування адалімумабу таким хворим (див. розділ «Побічні реакції»).
У всіх пацієнтів, особливо при інтенсивній імуносупресивній терапії в анамнезі, або у пацієнтів із псоріазом, яким проводили PUVA-терапію (псоралени з УФА), слід виключити наявність немеланомного раку шкіри до та протягом періоду застосування лікарського засобу Хайрімоз. Також повідомлялося про меланому та карциному з клітин Меркеля у пацієнтів, які отримували лікування антагоністами ФНП, включаючи адалімумаб (див. розділ «Побічні реакції»).
У пошуковому клінічному дослідженні, в якому оцінювали застосування іншого антагоніста ФНП (інфліксимаб), у пацієнтів із хронічною обструктивною хворобою легенів повідомлялося про більш часті випадки виникнення новоутворень, здебільшого у легенях, голові та на ділянці шиї, порівняно з контрольною групою. Всі пацієнти довгий час були курцями. Тому необхідно з обережністю застосовувати будь-які антагоністи ФНП пацієнтам із хронічною обструктивною хворобою легенів та пацієнтам із підвищеним ризиком виникнення новоутворень на тлі куріння.
На сьогодні невідомо, чи впливає застосування адалімумабу на ризик розвитку дисплазії або раку товстої кишки. Усі хворі на виразковий коліт, що входять до групи підвищеного ризику розвитку дисплазії або раку товстої кишки (зокрема пацієнти з довготривалим виразковим колітом або первинним склерозуючим холангітом), або ті, хто мав в анамнезі дисплазію або рак товстої кишки, повинні підлягати регулярному обстеженню щодо наявності дисплазії перед початком терапії та протягом перебігу всієї хвороби. Обстеження має включати колоноскопію та біопсію відповідно до місцевих рекомендацій.
Гематологічні розлади
При застосуванні блокаторів ФНП були поодинокі повідомлення про розвиток панцитопенії, апластичної анемії. При застосуванні адалімумабу (причинно-наслідковий зв’язок не з’ясований) повідомлялося про розвиток цитопенії (тромбоцитопенії, лейкопенії), що мала клінічне значення. Усіх пацієнтів потрібно попередити про необхідність негайної консультації лікаря при появі симптомів, притаманних захворюванням крові (таких як постійна гарячка, синці, кровотеча, блідість шкіри та слизових оболонок), на тлі застосування адалімумабу. Слід розглянути необхідність припинення застосування препарату Хайрімоз пацієнтам у разі підтвердження серйозних порушень з боку крові.
Вакцинація
Схожі реакції антитіл на стандартну 23-валентну пневмококову вакцину та тривалентну вакцину проти грипу спостерігалися в дослідженні за участю 226 дорослих пацієнтів з ревматоїдним артритом, які застосовували адалімумаб або плацебо. Відсутні дані щодо вторинної передачі інфекції живими вакцинами в пацієнтів, які отримували адалімумаб.
Для пацієнтів дитячого віку рекомендовано по можливості провести всі необхідні щеплення згідно з календарем до початку терапії препаратом Хайрімоз.
Пацієнтам під час застосування адалімумабу можна проводити вакцинацію, за винятком застосування живих вакцин. Застосування живих вакцин (наприклад вакцини БЦЖ) немовлятам, які піддавалися впливу адалімумабу внутрішньоутробно, не рекомендується протягом 5 місяців після останньої ін’єкції адалімумабу матері у період вагітності.
Хронічна серцева недостатність (ХСН)
У клінічному дослідженні з іншим антагоністом ФНП спостерігалося погіршення перебігу застійної серцевої недостатності та підвищення рівня пов’язаної з нею смертності. Також повідомлялося про випадки погіршення перебігу застійної серцевої недостатності у пацієнтів, які застосовували адалімумаб. Хайрімоз слід з обережністю застосовувати пацієнтам із серцевою недостатністю легкого ступеня тяжкості (клас I/II за класифікацією NYHA (Нью-Йоркська асоціація кардіологів)). Застосування лікарського засобу Хайрімоз протипоказане при серцевій недостатності помірного та тяжкого ступеня (див. розділ «Протипоказання»). При виникненні нових симптомів та погіршенні перебігу застійної серцевої недостатності лікування препаратом Хайрімоз слід припинити.
Аутоімунні процеси
Лікування адалімумабом може спричинити появу аутоантитіл. Вплив тривалого застосування препарату Хайрімоз на розвиток аутоімунних захворювань невідомий. При виникненні симптомів, що нагадують вовчакоподібний синдром, і виявленні антитіл до дволанцюгової ДНК подальше лікування препаратом Хайрімоз необхідно припинити (див. розділ «Побічні реакції»).
Одночасне застосування з біологічними DMARDs або з антагоністами ФНП
Спостерігалися серйозні інфекції під час клінічних досліджень супутнього застосування анакінри та етанерцепту, що не мало терапевтичних переваг у порівнянні з монотерапією етанерцептом. З огляду на характер побічних явищ, що спостерігалися під час комбінованого лікування етанерцептом та анакінрою, подібна токсичність може розвинутися при комбінації анакінри та іншого блокатора ФНП. Тому комбінація адалімумабу та анакінри не рекомендується (див. розділ «Взаємодія з іншими лікарськими засобами та інші види взаємодій»).
Одночасне застосування адалімумабу з іншими біологічними DMARDs (наприклад, анакінра та абатацепт) або з іншими антагоністами ФНП не рекомендується, зважаючи на можливе підвищення ризику інфекцій та інших потенційних фармакологічних взаємодій (див. розділ «Взаємодія з іншими лікарськими засобами та інші види взаємодій»).
Хірургічні втручання
Доступні обмежені дані щодо безпеки хірургічних процедур у пацієнтів, які отримують адалімумаб. Тривалий період напіввиведення адалімумабу необхідно брати до уваги, якщо планується хірургічне втручання. Пацієнта, який потребує хірургічного втручання та знаходиться на лікуванні препаратом Хайрімоз, потрібно ретельно обстежити на наявність інфекцій. У разі необхідності слід вжити відповідних заходів. Доступні обмежені дані щодо безпеки застосування пацієнтам, які піддавались артропластиці під час терапії адалімумабом.
Непрохідність тонкої кишки
Відсутність відповіді на лікування хвороби Крона може свідчити про наявність фіксованої фіброзної стриктури, яка вимагає лікування хірургічним шляхом. Доступні дані дають змогу вважати, що лікування адалімумабом не спричиняє виникнення або прогресування стриктур.
Пацієнти літнього віку
Частота розвитку серйозних інфекцій у пацієнтів віком від 65 років, які отримували адалімумаб (3,7 %), вища, ніж у молодших пацієнтів (1,5 %). Деякі випадки були летальними. У зв’язку з тим, що частота розвитку інфекцій у пацієнтів літнього віку вища, застосовувати адалімумаб пацієнтам цієї вікової категорії необхідно з обережністю.
Діти
Див. підрозділ «Вакцинація» вище.
Допоміжні речовини з відомими ефектами
Лікарський засіб Хайрімоз містить менше 1 ммоль натрію (23 мг) на 0,2 мл, тобто практично вільний від натрію.
Застосування у період вагітності або годування груддю
Жінки репродуктивного віку
Для запобігання вагітності жінки репродуктивного віку повинні користуватися надійними методами контрацепції під час лікування та протягом щонайменше п’яти місяців після введення останньої дози препарату Хайрімоз.
Вагітність
В результаті проспективного аналізу даних щодо застосування адалімумабу під час вагітності (приблизно 2100 випадків вагітностей, які завершилися народженням живих дітей з відомими наслідками, у тому числі понад 1500 випадків застосування препарату у першому триместрі) не виявлено збільшення частоти виникнення вад розвитку у новонароджених.
В проспективний когортний реєстр було включено 257 жінок з РА або ХК, які отримували адалімумаб як мінімум протягом першого триместру, та 120 жінок з РА або ХК, які не отримували адалімумаб. Первинною кінцевою точкою була частота розвитку значних вроджених вад у новонароджених. Частота випадків вагітностей, які завершилися народженням принаймні однієї живої дитини зі значною вродженою вадою, становила 6 з 69 (8,7 %) в групі жінок з РА, які отримували адалімумаб, та 5 з 74 (6,8 %) – в групі жінок з РА, які не застосовували препарат (нескориговане відношення шансів [ВШ] 1,31, 95 % довірчий інтервал [ДІ] 0,38–4,52). В групі жінок з ХК, які отримували адалімумаб, частота таких випадків становила 16 зі 152 (10,5 %), а в групі жінок з ХК, які не застосовували препарат, відповідно 3 з 32 (9,4 %) (нескориговане ВШ 1,14, 95 % ДІ 0,31–4,16). В об’єднаній групі жінок з РА та ХК скориговане ВШ (з поправкою на відмінності на вихідному рівні) становило 1,10 (95 % ДІ 0,45–2,73). Між жінками, які застосовували та не застосовували адалімумаб, не було виявлено чітко виражених відмінностей щодо вторинних кінцевих точок у вигляді спонтанних абортів, незначних вроджених вад, передчасних пологів, маси тіла та зросту новонароджених і серйозних або опортуністичних інфекцій, а також не було зареєстровано випадків мертвонародження або розвитку злоякісних пухлин. На інтерпретацію даних могли впливати методологічні обмеження дослідження, у тому числі малий об’єм вибірки та нерандомізований дизайн дослідження.
В експериментальному дослідженні токсичності на мавпах не було виявлено ознак токсичної дії на материнський організм, а також ембріотоксичної та тератогенної дії. Доклінічні дані щодо постнатальної токсичності адалімумабу відсутні.
Оскільки адалімумаб інгібує ФНП-α, його застосування під час вагітності може порушити нормальні імунні реакції у новонародженого. Вагітним жінкам слід застосовувати адалімумаб лише у разі очевидної необхідності.
Адалімумаб може проникати через плаценту в сироватку крові новонароджених, матері яких отримували адалімумаб під час вагітності. Тому у таких новонароджених може бути підвищений ризик інфікування. Застосування живих вакцин (наприклад вакцини БЦЖ) немовлятам, що піддавалися впливу адалімумабу внутрішньоутробно, не рекомендується протягом 5 місяців після останньої ін’єкції адалімумабу матері у період вагітності.
Годування груддю
Обмежені опубліковані дані свідчать про те, що адалімумаб екскретується у грудне молоко у дуже низьких концентраціях – від 0,1 % до 1 % від рівня у сироватці матері. Враховуючи те, що білки імуноглобуліну G піддаються в кишечнику протеолізу і мають низьку біодоступність, системний вплив адалімумабу на немовлят, які знаходяться на грудному вигодовуванні, малоймовірний. Отже, препарат Хайрімоз можна застосовувати в період годування груддю.
Фертильність
Доклінічні дані щодо впливу адалімумабу на фертильність відсутні.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Хайрімоз може мати незначний вплив на швидкість реакції при керуванні автотранспортом або іншими механізмами. Застосування лікарського засобу Хайрімоз може спричинити виникнення вертиго та порушення гостроти зору (див. розділ «Побічні реакції»).
Спосіб застосування та дози
Терапію препаратом Хайрімоз повинен призначати лікар, який має досвід діагностування та терапії захворювань, при яких показаний Хайрімоз. Офтальмологам рекомендовано проконсультуватися з відповідним спеціалістом перед тим, як призначати терапію препаратом Хайрімоз. Пацієнти, які застосовують лікарський засіб Хайрімоз, повинні отримати картку-пам’ятку пацієнта.
Хайрімоз можна вводити самостійно тільки у разі, якщо пацієнт або батьки дитини, якій призначена терапія адалімумабом, пройшли відповідний інструктаж у лікаря щодо техніки введення ін’єкції та лікар підтвердив, що це можливо. Додатково необхідно ознайомитись з інформацією щодо самостійного введення, яка міститься в цій інструкції. Під час лікування препаратом Хайрімоз інші супутні види терапії (наприклад терапію кортикостероїдами та/або імуномодулюючими препаратами) потрібно переглянути.
Ревматоїдний артрит
Рекомендована доза для дорослих пацієнтів становить 40 мг 1 раз на 2 тижні підшкірно. Під час терапії лікарським засобом Хайрімоз необхідно продовжувати застосовувати метотрексат, також можна продовжувати терапію глюкокортикоїдами, саліцилатами, нестероїдними протизапальними препаратами, аналгетиками. Щодо застосування інших протиревматичних препаратів, які модифікують перебіг захворювання (DMARDs), див. розділ «Особливості застосування».
Для деяких хворих на РА, які не застосовують метотрексат, може бути виправданим збільшення частоти введення препарату до 40 мг 1 раз на тиждень підшкірно або 80 мг 1 раз на 2 тижні.
Клінічна відповідь зазвичай досягається протягом 12 тижнів лікування. Слід переглянути необхідність продовження терапії для пацієнтів, у яких протягом вказаного терміну не спостерігається відповіді на лікування.
Якщо необхідно, можна перервати терапію (наприклад, перед хірургічним втручанням або у разі тяжкої інфекції). Існують дані, що після повернення до терапії через 70 днів або більше клінічна відповідь та профіль безпеки є подібними до тих, що були до перерви.
Аксіальний спондилоартрит (анкілозуючий спондиліт та аксіальний спондилоартрит без рентгенологічного підтвердження АС) та псоріатичний артрит
Рекомендована доза для дорослих пацієнтів становить 40 мг 1 раз на 2 тижні підшкірно.
Клінічна відповідь зазвичай досягається протягом 12 тижнів лікування. Слід переглянути необхідність продовження терапії для пацієнтів, у яких протягом вказаного терміну не спостерігається відповіді на лікування.
Бляшковий псоріаз
Рекомендована початкова доза для дорослих становить 80 мг, через 1 тиждень застосовувати 40 мг підшкірно. Підтримуюча терапія – 40 мг 1 раз на 2 тижні підшкірно.
Слід ретельно переглянути необхідність продовження терапії після 16 тижнів для пацієнтів, у яких протягом вказаного терміну не спостерігається відповіді на лікування.
Для пацієнтів, у яких не спостерігається адекватної відповіді на Хайрімоз в дозі 40 мг 1 раз на 2 тижні протягом 16 тижнів терапії, може бути ефективним підвищення дози до 40 мг 1 раз на тиждень або 80 мг 1 раз на 2 тижні. Слід ретельно переглянути співвідношення користь/ризик продовження терапії в дозі 40 мг на тиждень або 80 мг 1 раз на 2 тижні для пацієнтів, у яких не було адекватної відповіді на лікування після підвищення дози (див. розділ «Фармакодинаміка»). Якщо була досягнута адекватна відповідь після переходу на 40 мг на тиждень або 80 мг 1 раз на 2 тижні, дозу потім можна зменшити до 40 мг 1 раз на 2 тижні.
Гнійний гідраденіт (ГГ)
Рекомендований режим дозування для дорослих пацієнтів з гнійним гідраденітом – 160 мг початково на тижні 0 (день 1), дозу можна вводити у вигляді 4 ін’єкцій в один день або по 2 ін’єкції в день протягом двох днів поспіль, потім – 80 мг через 2 тижні (день 15), дозу слід вводити у вигляді 2 ін’єкцій в один день. По закінченню двох тижнів (день 29) рекомендована доза становить 40 мг 1 раз на тиждень. Протягом терапії препаратом Хайрімоз можна продовжувати приймати антибіотики, якщо це необхідно. Також рекомендовано продовжувати щоденне місцеве промивання антисептиками уражених ділянок.
Слід ретельно переглянути необхідність продовження терапії понад 12 тижнів для пацієнтів, у яких у межах цього терміну не спостерігається клінічної відповіді.
При перериванні терапії можливе повернення до застосування адалімумабу в дозі 40 мг 1 раз на тиждень або 80 мг 1 раз на 2 тижні (див. розділ «Фармакодинаміка»).
При довготривалій терапії необхідно періодично оцінювати співвідношення користь/ризик (див. розділ «Фармакодинаміка»).
Хвороба Крона
Для індукції ремісії рекомендована початкова доза для дорослих пацієнтів становить 80 мг на тижні 0 (день 1) з подальшим зменшенням дози до 40 мг на тижні 2 (день 15) підшкірно. Якщо необхідно отримати більш швидку клінічну відповідь, можна спочатку застосовувати 160 мг на тижні 0 (день 1), доза може бути введена у вигляді 4-х ін’єкцій в один день або як дві ін’єкції по 40 мг протягом двох днів поспіль, а на тижні 2 (день 15) застосовувати дозу 80 мг підшкірно. Необхідно взяти до уваги, що у такому випадку ризик виникнення побічних реакцій підвищується.
Після індукційної терапії розпочинати підтримуюче лікування у дозі 40 мг 1 раз на 2 тижні підшкірно. Альтернативно, якщо пацієнт припинив терапію і знову з’явилися симптоми захворювання, терапію лікарським засобом Хайрімоз можна розпочати знову. Існують обмежені дані щодо повторної терапії лікарським засобом Хайрімоз після перерви більше ніж на 8 тижнів від введення останньої дози. Протягом підтримуючої терапії дозу кортикостероїдів можна зменшити, зважаючи на клінічну практику.
При зменшенні клінічної відповіді деякі пацієнти можуть потребувати збільшення частоти введення препарату до 40 мг 1 раз на тиждень підшкірно або 80 мг 1 раз на 2 тижні.
Деяким пацієнтам, у яких не досягнуто клінічної відповіді на 4-й тиждень лікування, слід продовжити підтримуючу терапію до 12-го тижня. Слід ретельно переглянути необхідність продовження терапії для пацієнтів, у яких в межах цього терміну не спостерігається клінічної відповіді.
Виразковий коліт
Рекомендована початкова доза для індукції ремісії у дорослих пацієнтів з виразковим колітом помірного або тяжкого ступеня активності становить 160 мг на тижні 0 (день 1), доза може бути введена у вигляді 4-х ін’єкцій в один день або по дві ін’єкції в день протягом двох днів поспіль, та 80 мг через 2 тижні (день 15). Після індукційної терапії рекомендована доза становить 40 мг 1 раз на 2 тижні у вигляді підшкірної ін’єкції.
Протягом підтримуючої терапії дозу кортикостероїдів можна зменшити, зважаючи на клінічну практику.
При зменшенні клінічної відповіді деякі пацієнти можуть потребувати збільшення частоти введення препарату до 40 мг 1 раз на тиждень або 80 мг 1 раз на 2 тижні.
Клінічна відповідь має бути досягнута протягом 2–8 тижнів лікування. Терапію препаратом Хайрімоз можна продовжувати тільки для тих пацієнтів, які досягли клінічної відповіді протягом перших 8-ми тижнів лікування.
Увеїт
Рекомендована початкова доза препарату Хайрімоз для дорослих пацієнтів з увеїтом становить 80 мг, починаючи з першого тижня після початкової дози необхідно перейти до підтримуючої терапії – 40 мг 1 раз на 2 тижні підшкірно.
Існують обмежені дані щодо введення лише адалімумабу як стартової терапії. Терапію препаратом Хайрімоз можна розпочати в комбінації з кортикостероїдами та/або з іншими небіологічними імуномодулюючими препаратами. Через 2 тижні після початку комбінованої терапії поступово можна перейти на монотерапію препаратом Хайрімоз відповідно до клінічного досвіду.
Рекомендовано щорічно оцінювати співвідношення користь/ризик довготривалої терапії.
Особливі групи пацієнтів
Пацієнти літнього віку
Змінювати дозу препарату не потрібно.
Пацієнти з порушенням функції печінки та/або нирок
Застосування адалімумабу таким пацієнтам не досліджувалось, тому рекомендації щодо дозування відсутні.
Діти
Ювенільний ревматоїдний (ідіопатичний) артрит (ЮРА)
Поліартикулярний ювенільний ревматоїдний (ідіопатичний) артрит
Рекомендована доза лікарського засобу Хайрімоз для дітей віком від 2 років з поліартикулярною формою ЮРА залежить від маси тіла (таблиця 1). Хайрімоз застосовують 1 раз на 2 тижні підшкірно.
Таблиця 1. Дозування препарату Хайрімоз для пацієнтів з поліартикулярною формою ЮРА
|
Маса тіла |
Доза |
|
10 кг до 30 кг |
20 мг 1 раз на 2 тижні |
|
30 кг та більше |
40 мг 1 раз на 2 тижні |
Клінічна відповідь згідно з існуючими даними зазвичай досягається протягом 12 тижнів лікування. Слід переглянути необхідність продовження терапії для пацієнтів, у яких протягом вказаного терміну не спостерігається відповіді на лікування.
Хайрімоз не застосовують за цим показанням дітям віком до 2 років.
Ентезитасоційований артрит
Рекомендована доза лікарського засобу Хайрімоз для дітей віком від 6 років залежить від маси тіла (таблиця 2). Хайрімоз застосовують 1 раз на 2 тижні підшкірно.
Таблиця 2. Дозування Хайрімоз для пацієнтів з ентезитасоційованим артритом
|
Маса тіла |
Доза |
|
15 кг до 30 кг |
20 мг 1 раз на 2 тижні |
|
30 кг та більше |
40 мг 1 раз на 2 тижні |
Застосування лікарського засобу Хайрімоз дітям віком до 6 років з ентезитасоційованим артритом не вивчалось.
Бляшковий псоріаз у дітей
Рекомендована доза препарату Хайрімоз для пацієнтів віком від 4 до 17 років з бляшковим псоріазом залежить від маси тіла (таблиця 3). Хайрімоз застосовують підшкірно.
Таблиця 3. Дозування Хайрімоз для дітей з бляшковим псоріазом
|
Маса тіла |
Доза |
|
15 кг до 30 кг |
Початкова доза становить 20 мг на тижні 0, потім 20 мг 1 раз на 2 тижні, починаючи з тижня 1 |
|
30 кг і більше |
Початкова доза становить 40 мг на тижні 0, потім 40 мг 1 раз на 2 тижні, починаючи з тижня 1 |
Слід ретельно переглянути необхідність продовження терапії для пацієнтів, у яких протягом 16 тижнів не спостерігається клінічної відповіді.
Якщо призначено повторну терапію препаратом Хайрімоз, необхідно дотримуватись схеми лікування, зазначеної вище.
Безпека застосування адалімумабу дітям з бляшковим псоріазом вивчалась в середньому протягом 13 місяців.
Застосування адалімумабу дітям віком до 4 років з бляшковим псоріазом не вивчалось.
Гідраденіт у дітей віком від 12 років та з масою тіла не менше 30 кг Немає клінічних досліджень щодо застосування адалімумабу дітям віком від 12 років з гідраденітом. Дозування адалімумабу таким пацієнтам було визначено методом фармакокінетичного моделювання та симуляції (див. розділ «Фармакокінетика»).
Рекомендована доза адалімумабу становить 80 мг початково на тижні 0, потім 40 мг 1 раз на 2 тижні, починаючи з тижня 1, підшкірно.
Для пацієнтів з недостатньою відповіддю на застосування адалімумабу 40 мг 1 раз на 2 тижні може бути доцільним підвищення частоти застосування дози 40 мг до 1 разу на тиждень. Протягом терапії препаратом Хайрімоз можна продовжувати приймати антибіотики, якщо це необхідно. Також рекомендовано продовжувати щоденне місцеве промивання антисептиками уражених ділянок.
Слід ретельно переглянути необхідність продовження терапії понад 12 тижнів для пацієнтів, у яких у межах цього терміну не спостерігається клінічної відповіді.
При перериванні терапії можливе повернення до застосування препарату Хайрімоз, якщо це необхідно.
При довготривалій терапії необхідно періодично оцінювати співвідношення користь/ризик (див. дані для дорослих у розділі «Фармакодинаміка»).
Адалімумаб не застосовують за цим показанням дітям віком до 12 років.
Хвороба Крона у дітей
Рекомендована доза препарату Хайрімоз для пацієнтів віком від 6 до 17 років з хворобою Крона залежить від маси тіла (таблиця 4).
Хайрімоз застосовують підшкірно.
Таблиця 4. Дозування препарату Хайрімоз для дітей із хворобою Крона
|
Маса тіла |
Індукційна доза |
Підтримуюча терапія, починаючи з тижня 4 |
|
< 40 кг |
40 мг на тижні 0 та 20 мг на тижні 2 Якщо існує потреба в більш швидкій відповіді на терапію, можна використовувати таку схему: 80 мг на тижні 0 та 40 мг на тижні 2. Але слід враховувати, що ризик побічних явищ при застосуванні більш високої індукційної дози зростає. |
20 мг 1 раз на 2 тижні |
|
≥ 40 кг |
80 мг на тижні 0 та 40 мг на тижні 2 Якщо існує потреба в більш швидкій відповіді на терапію, можна використовувати таку схему: 160 мг на тижні 0 та 80 мг на тижні 2. Але слід враховувати, що ризик побічних явищ при застосуванні більш високої індукційної дози зростає. |
40 мг 1 раз на 2 тижні |
Для пацієнтів з недостатньою відповіддю може бути доцільним збільшення частоти застосувань препарату Хайрімоз:
пацієнтам з масою тіла < 40 кг: 20 мг 1 раз на тиждень;
пацієнтам з масою тіла ≥ 40 кг: 40 мг 1 раз на тиждень або 80 мг 1 раз на 2 тижні.
Слід ретельно переглянути необхідність продовження терапії для пацієнтів, у яких протягом 12 тижнів не спостерігається клінічної відповіді.
Хайрімоз не застосовують за цим показанням дітям віком до 6 років.
Виразковий коліт (ВК) у дітей
Рекомендована доза препарату Хайрімоз для пацієнтів віком від 6 до 17 років з виразковим колітом базується на масі тіла (таблиця 5). Хайрімоз вводять шляхом підшкірної ін’єкції.
Таблиця 5. Дозування препарату Хайрімоз для дітей з виразковим колітом (ВК)
|
Маса тіла |
Доза |
Підтримуюча терапія, починаючи з тижня 4* |
|
< 40 кг |
80 мг на 0-му тижні (у вигляді двох ін’єкцій по 40 мг в один день) 40 мг на 2-му тижні (вводиться як одна ін’єкція 40 мг) |
40 мг через тиждень |
|
≥ 40 кг |
160 мг на тижні 0 (у вигляді чотирьох ін’єкцій по 40 мг ін’єкції в один день або дві ін’єкції по 40 мг на добу два дні поспіль) 80 мг на 2-му тижні (у вигляді двох ін’єкцій по 40 мг в один день) |
80 мг кожні два тижні (у вигляді двох ін’єкцій по 40 мг в один день) |
* Пацієнти, яким виповнюється 18 років під час лікування препаратом Хайрімоз, повинні продовжувати лікування підтримуючою терапією.
Слід ретельно переглянути необхідність продовження терапії для пацієнтів, у яких протягом 8 тижнів не спостерігається клінічної відповіді.
Застосування лікарського засобу Хайрімоз дітям віком до 6 років з виразковим колітом не вивчалось.
Лікарський засіб Хайрімоз доступний в інших дозуваннях залежно від індивідуальних потреб в лікуванні.
Увеїт у дітей
Рекомендована доза лікарського засобу Хайрімоз для дітей віком від 2 років з хронічним неінфекційним увеїтом залежить від маси тіла (таблиця 6). Хайрімоз застосовують підшкірно.
Немає даних щодо застосування адалімумабу без супутньої терапії метотрексатом дітям з увеїтом.
Таблиця 6. Дозування лікарського засобу Хайрімоз дітям з увеїтом
|
Маса тіла |
Доза |
|
до 30 кг |
20 мг 1 раз на 2 тижні в комбінації з метотрексатом |
|
30 кг і більше |
40 мг 1 раз на 2 тижні в комбінації з метотрексатом |
Початкова навантажувальна доза адалімумабу становить 40 мг для пацієнтів з масою тіла до 30 кг і 80 мг для пацієнтів, маса тіла яких 30 кг і більше; її можна ввести за тиждень до початку підтримуючої терапії. Немає клінічних даних щодо введення початкової навантажувальної дози адалімумабу дітям віком до 6 років (див. розділ «Фармакокінетика»).
Застосовування Хайрімоз дітям віком до 2 років за даним показанням не обґрунтоване. Рекомендується щорічно оцінювати користь та ризик довготривалого лікування (див. розділ «Фармакодинаміка»).
Псоріатичний артрит та аксіальний спондилоартрит, включаючи анкілозуючий спондиліт
Застосування адалімумабу дітям за показаннями анкілозуючий спондиліт та псоріатичний артрит не є релевантним.
Спосіб застосування
Хайрімоз застосовують підшкірно.
Введення
Щоб уникнути можливого інфікування й забезпечити правильне використання лікарського засобу, неухильно дотримуйтеся цих інструкцій.
Перед введенням препарату Хайрімоз обов’язково прочитайте ці інструкції із застосування лікарського засобу, переконайтеся, що вам усе зрозуміло, та дотримуйтеся їх. Переш ніж ви почнете використовувати препарат Хайрімоз, ваш лікар покаже, як підготуватися та зробити ін’єкцію попередньо наповненим шприцом із однією дозою. З усіма запитаннями звертайтеся до свого лікаря.
Попередньо наповнений шприц із однією дозою препарату Хайрімоз
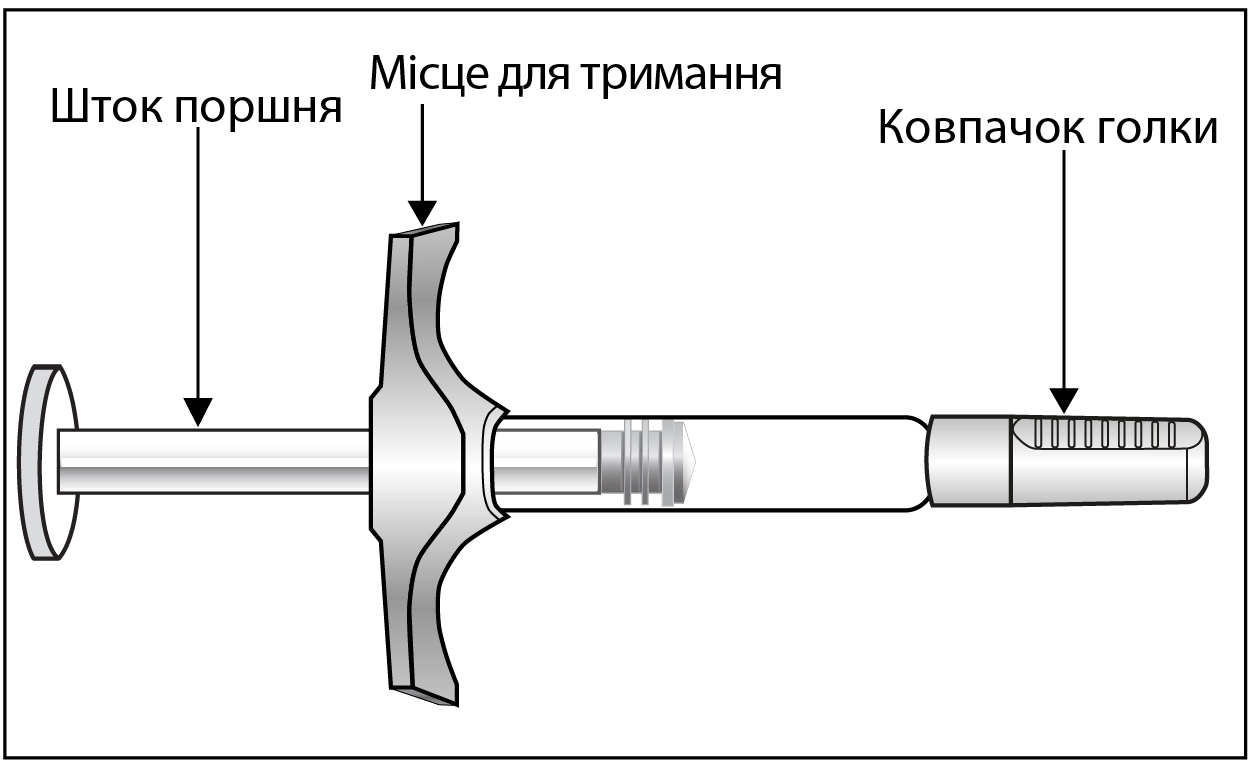
|
|
Рис. A. Попередньо наповнений шприц із препаратом Хайрімоз |
Обов’язково дотримуйтесь таких інструкцій:
· Не використовуйте попередньо наповнений шприц, якщо пломби блістера порушені, оскільки це може бути небезпечно.
· Не відкривайте зовнішню упаковку, доки не будете готові до використання попередньо наповненого шприца з лікарським засобом Хайрімоз.
· Ніколи не залишайте попередньо наповнений шприц без нагляду там, де інші особи можуть мати до нього доступ.
· Якщо ви впустили шприц, не використовуйте його в разі пошкодження або від’єднання ковпачка.
· Не знімайте ковпачок, доки не будете готові до ін’єкції.
· Вводьте Хайрімоз через 15–30 хвилин після виймання з холодильника для більш комфортного введення.
· Негайно викиньте шприц після використання. Не використовуйте шприц повторно. Див. п. 4. «Утилізація використаних шприців».
· Запитайте в лікаря або медсестри, у яку ділянку та яким чином робити ін’єкцію, якщо у вас мала маса тіла або ви робите ін’єкцію дитині.
· Зберігайте попередньо наповнений шприц із препаратом Хайрімоз в оригінальній упаковці для захисту від світла.
· Зберігайте зовнішню упаковку з попередньо наповненими шприцами в холодильнику при температурі 2–8 °С.
· За потреби (наприклад, на час подорожі) попередньо наповнений шприц можна зберігати за кімнатної температури (до 25 °С) не довше 42 днів.
· Викиньте попередньо наповнений шприц, якщо він зберігався за кімнатної температури довше 42 днів.
· Запишіть дату, коли шприц був вперше вийнятий із холодильника, і дату, після якої його потрібно викинути.
· Не зберігайте попередньо наповнений шприц за критично високих або критично низьких температур.
· Не заморожуйте попередньо наповнений шприц.
· Не використовуйте попередньо наповнений шприц після завершення його терміну придатності, який зазначений на зовнішній упаковці або маркуванні шприца. Якщо термін придатності сплив, поверніть усю упаковку провізору.
Зберігайте препарат Хайрімоз і всі лікарські засоби в недоступному для дітей місці.
Що потрібно для ін’єкції?
Розкладіть зазначені нижче предмети на чистій рівній поверхні.
Вміст упаковки з попередньо наповненим шприцом:
· Попередньо наповнений шприц із препаратом Хайрімоз (див. рис. А). Кожен попередньо наповнений шприц містить 20 мг / 0,2 мл адалімумабу.
Не входить до складу упаковки з попередньо наповненим шприцом із препаратом Хайрімоз (див. рис. В):
· Спиртова серветка
· Ватна кулька або бинт
· Контейнер для гострих предметів; див. п. 4 «Утилізація використаних шприців»
· Пластир
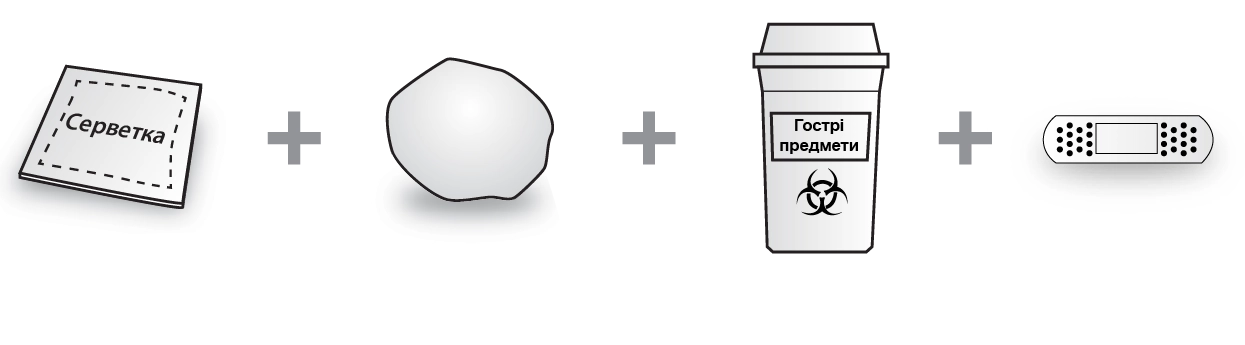
Рис. В. Предмети, що не входять до складу упаковки
Підготовка попередньо наповненого шприца
· Для більш комфортної ін’єкції дістаньте з холодильника упаковку з попередньо наповненим шприцом і залиште її невідкритою на робочій поверхні приблизно на 15–30 хвилин до досягнення кімнатної температури.
· Дістаньте попередньо наповнений шприц із коробки й огляньте його. Розчин повинен бути безбарвним або злегка жовтуватим, а також прозорим або злегка опалесцентним. Не використовуйте препарат, якщо в ньому спостерігаються частинки та/або наявна зміна кольору. Якщо вас турбує зовнішній вигляд розчину, зверніться за допомогою до провізора.
· Не використовуйте попередньо наповнений шприц, якщо він пошкоджений. Поверніть шприц разом з упаковкою до аптеки.
· Перевірте термін придатності (Прид. до) на попередньо наповненому шприці. Не використовуйте попередньо наповнений шприц, якщо термін придатності сплив.
|
1. Вибір місця ін’єкції |
|
|
Місце ін’єкції – це ділянка тіла, у яку ви будете вводити препарат Хайрімоз із попередньо наповненого шприца. · Рекомендованим місцем ін’єкції є передня частина стегон. Також препарат можна вводити у нижню частину живота, але в радіусі не менше ніж 5 см навколо пупка (див. рис. C). · Щоразу обирайте інше місце ін’єкції. · Не вводьте препарат у зони, де шкіра є чутливою, має синці, почервоніння, лущення або ущільнення. Уникайте ділянок зі шрамами або розтяжками. · Якщо у вас псоріаз, не вводьте препарат безпосередньо в зони з бляшками. |
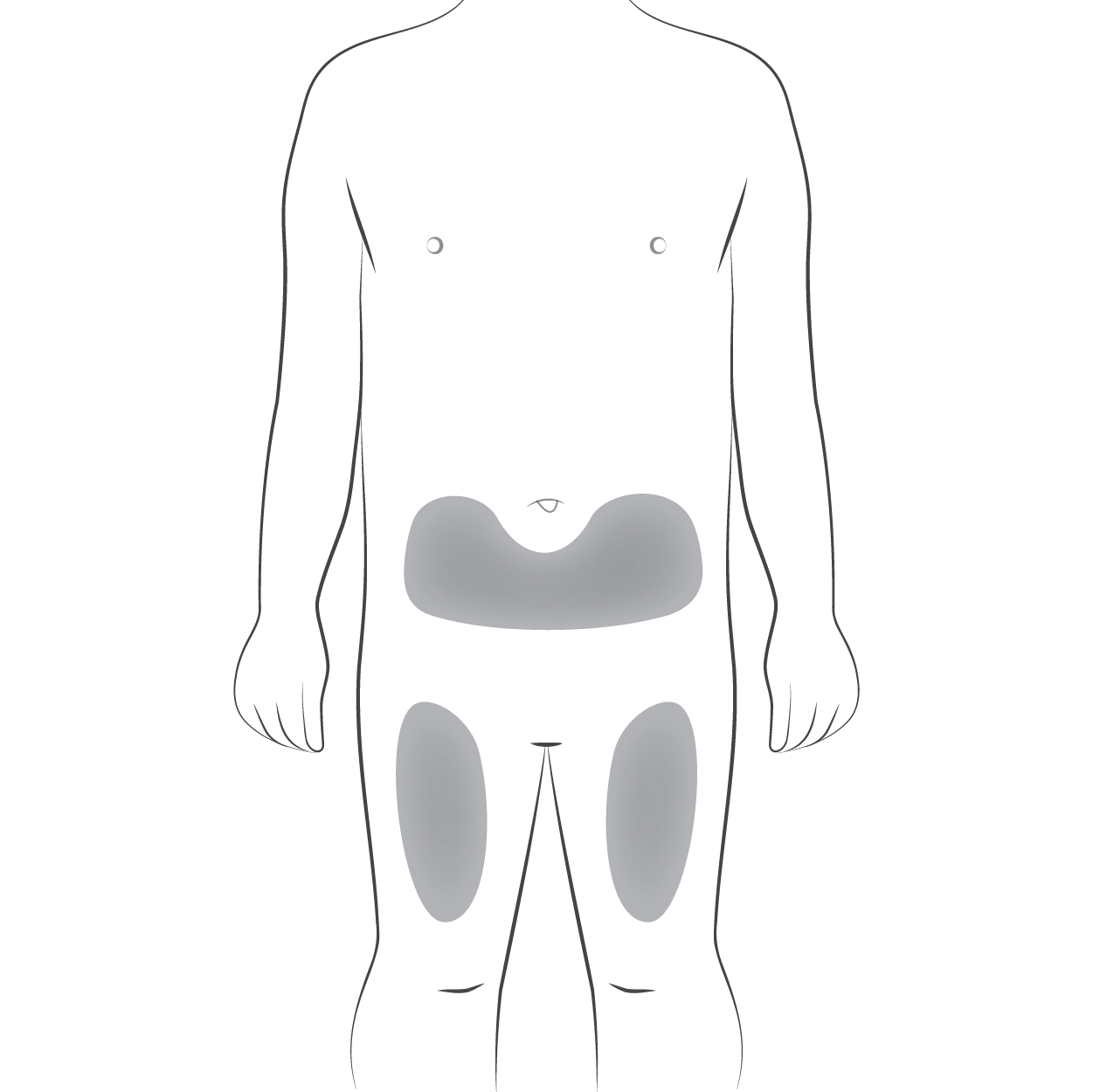 Рис. C. Вибір місця ін’єкції
Рис. C. Вибір місця ін’єкції
|
|
2. Очищення місця ін’єкції |
|
|
· Добре вимийте руки водою з милом, коли будете готові використовувати попередньо наповнений шприц. · Круговими рухами протріть місце ін’єкції спиртовою серветкою. Дайте висохнути (див. рис. D). · Не торкайтесь очищеної ділянки перед ін’єкцією. Почекайте, доки шкіра висохне. Не сушіть очищену ділянку феном і не дмухайте на неї. |

Рис. D. Очищення місця ін’єкції |
|
3. Процедура ін’єкції |
|
|
· Обережно змініть ковпачок зі шприца, не нахиляючи його в жодний бік (див. рис. E). · Викиньте ковпачок. · Ви можете побачити краплю рідини на кінці голки. Це нормально. |
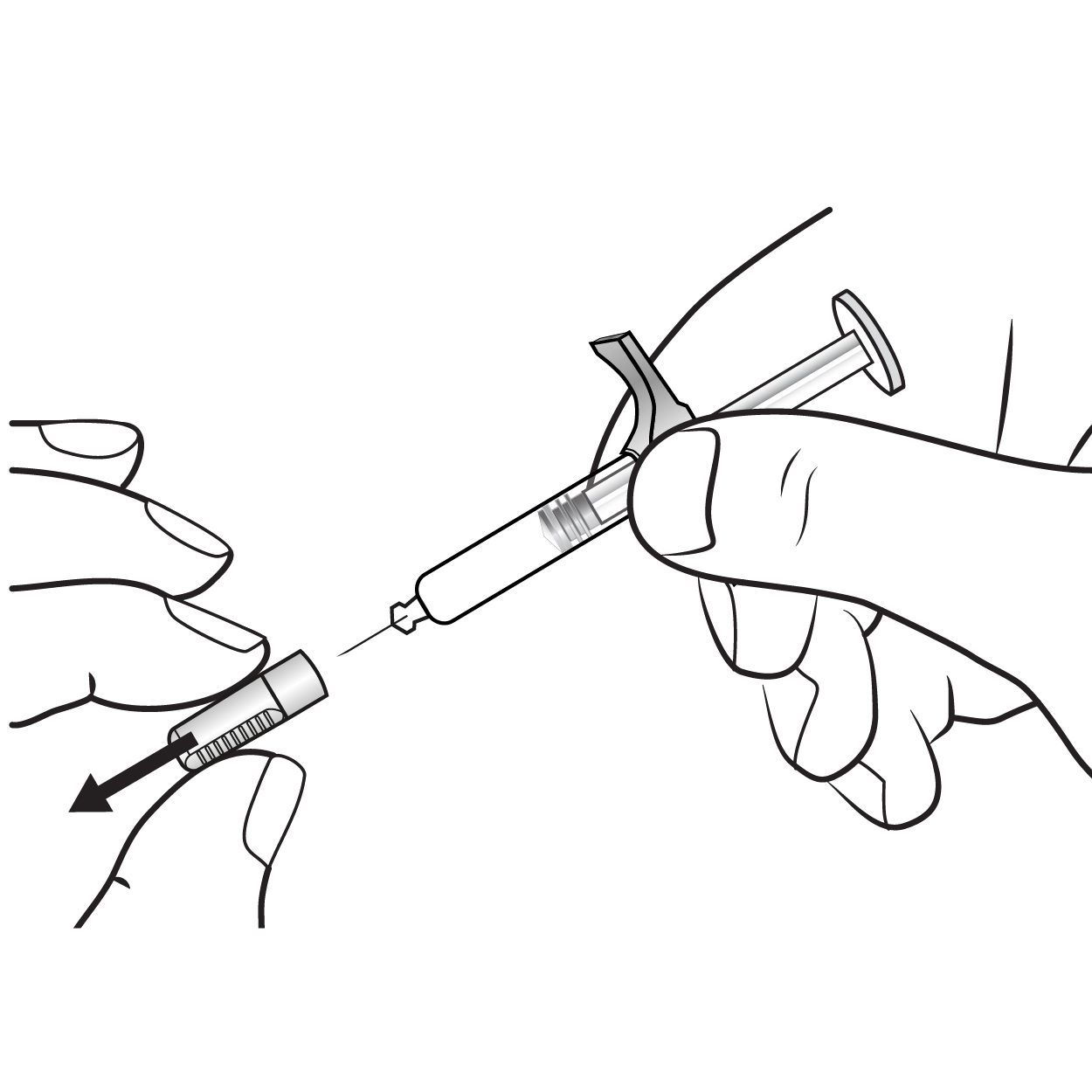
Рис. E. Зняття ковпачка |
|
· Обережно прищипніть шкіру у місці ін’єкції (див. рис. F). · Введіть голку в шкіру під кутом 45 градусів, як показано на зображенні (див. рис. F). |

Рис. F. Введення голки |
|
· Тримайте попередньо наповнений шприц, як показано на зображенні (див. рис. G). · Повільно натискайте на поршень до кінця руху. · Тримайте поршень натиснутим, утримуючи шприц на місці протягом 5 секунд. · Обережно витягніть голку зі шкіри, тримаючи шприц вертикально. Із місця проколу може виступити крапля крові. Притисніть ватну кульку або бинт до місця ін’єкції та потримайте 10 хвилин. Не тріть місце ін’єкції. За потреби можна наклеїти пластир. |

Рис. G. Утримування поршня |
|
4. Утилізація використаних шприців |
|
|
· Викиньте використаний шприц у контейнер для гострих предметів (контейнер зі стійкого до проколів матеріалу із кришкою). Для власної безпеки та захисту оточуючих ніколи не використовуйте шприци й голки повторно. · Ніколи не викидайте лікарські засоби в каналізацію або разом із побутовими відходами. Запитайте лікаря або провізора, як правильно позбутися ліків, які вам більше не потрібні. Ці заходи допоможуть захистити довкілля. Усі невикористані засоби або відходи слід утилізувати з дотриманням вимог місцевого законодавства. |
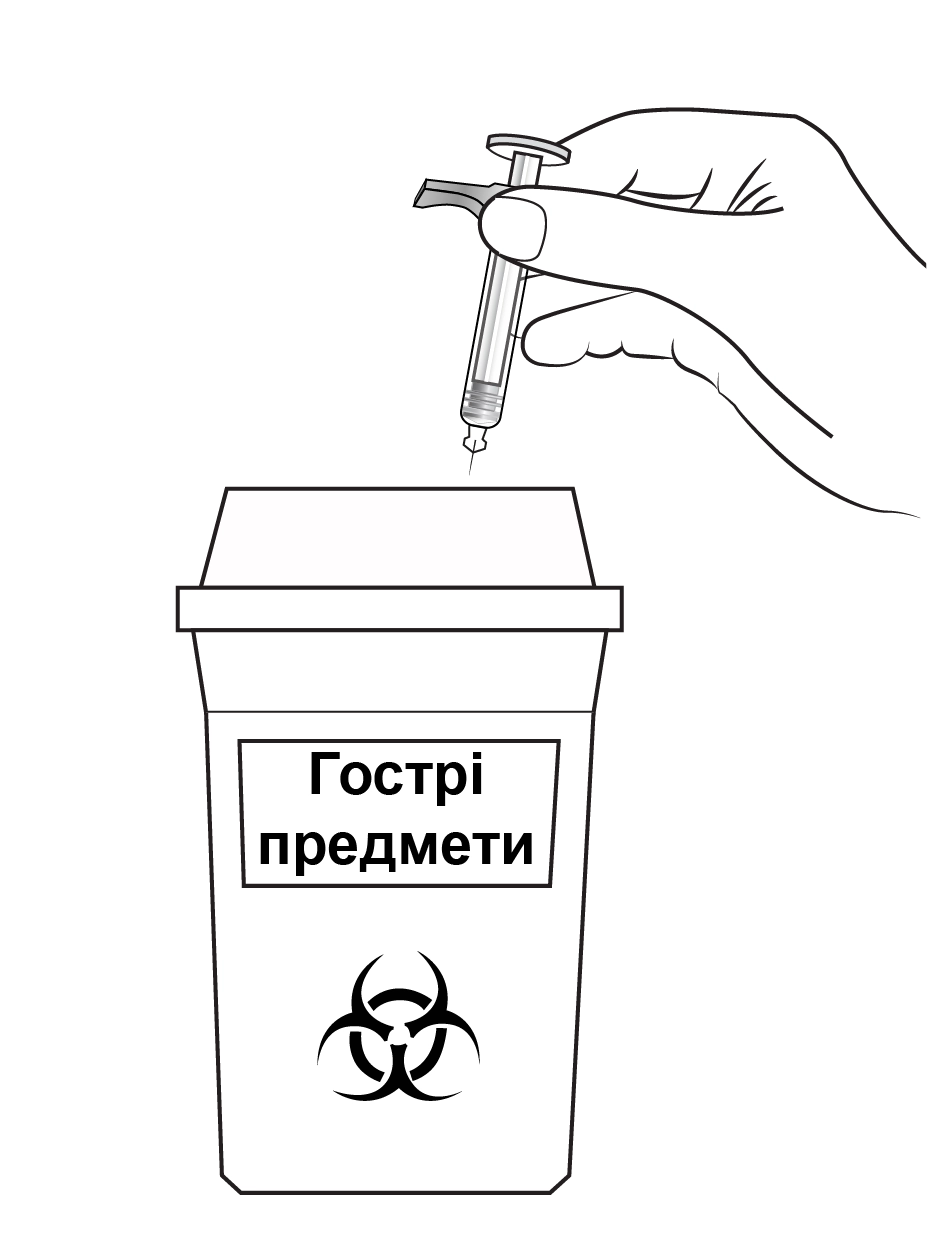
Рис. H. Утилізація використаного попередньо наповненого шприца |
Якщо у вас виникли запитання, зверніться до свого лікаря, провізора або медсестри, які знайомі з особливостями використання препарату Хайрімоз.
Попередньо наповнений шприц може зберігатися при температурі максимум до 25 °C протягом періоду до 42 днів. Попередньо наповнений шприц слід зберігати у захищеному від світла місці та утилізувати, якщо він не використовується протягом 42-денного періоду.
Діти
Показаний для застосування дітям згідно з розділом «Показання».
Передозування
У ході клінічних досліджень адалімумабу не було виявлено випадків дозолімітуючої токсичності. Пацієнтам призначалися багаторазові дози до 10 мг/кг, що приблизно в 15 разів більше рекомендованої дози. Таке застосування не супроводжувалось ознаками токсичності, пов’язаної із передозуванням.
Побічні реакції
Загальна інформація щодо профілю безпеки
Адалімумаб досліджували у контрольованих клінічних дослідженнях та дослідженнях відкритого періоду тривалістю близько 60 місяців чи більше за участю 9506 пацієнтів. Ці дослідження включали пацієнтів з раннім та довготривалим ревматоїдним артритом, ЮРА (поліартикулярним ювенільним ідіопатичним артритом та ентезитасоційованим артритом), а також із аксіальним спондилоартритом (анкілозуючий спондиліт та нерентгенографічний аксіальний спондилоартрит), псоріатичним артритом, хворобою Крона, виразковим колітом, псоріазом, гнійним гідраденітом, увеїтом. Нижче приведено дані, отримані під час основних контрольованих досліджень, в яких 6089 пацієнтам застосовували адалімумаб та 3801 пацієнту застосовували плацебо або препарат порівняння впродовж контрольованого періоду.
Протягом основних клінічних випробувань 5,9 % пацієнтів, які отримували адалімумаб, та 5,4 % пацієнтів з контрольної групи припинили лікування через побічні реакції.
Найчастіше повідомлялось про виникнення побічних реакцій у вигляді інфекцій (таких як назофарингіт, інфекції верхніх відділів дихальних шляхів та синусит), реакцій в місці введення (почервоніння, свербіж, геморагії, біль або набряк), головний біль та скелетно-м’язовий біль.
Повідомлялося про серйозні побічні реакції при застосуванні адалімумабу. Антагоністи ФНП, такі як Хайрімоз, впливають на імунну систему, їх застосування може спричинити зниження опірності організму до інфекцій та злоякісних новоутворень.
Під час застосування адалімумабу повідомлялося про виникнення інфекцій, які можуть становити загрозу життю людини та призвести до смерті (включаючи сепсис, опортуністичні інфекції та туберкульоз), про реактивацію гепатиту В та виникнення різних новоутворень (включаючи лейкемію, лімфому та гепатолієнальну Т-клітинну лімфому).
Повідомлялось також про серйозні гематологічні, неврологічні та аутоімунні реакції. Ці реакції включали поодинокі випадки панцитопенії, апластичної анемії, випадки центральних та периферичних демієлінізуючих розладів, виникнення вовчака, вовчакоподібних станів та синдрому Стівенса – Джонсона.
Діти
Зазвичай побічні реакції, що виникали у дітей, були однакові за частотою та характером з побічними реакціями, які спостерігалися у дорослих пацієнтів.
У таблиці 7 представлено побічні реакції з можливим причинно-наслідковим зв’язком, які спостерігалися протягом клінічних випробувань та у постмаркетинговий період. Побічні реакції зазначено за органами і системами організму та частотою виникнення (≥ 1/10 – дуже часті, від ≥1/100 до ˂1/10 – часті; від ≥ 1/1000 до ˂1/100 – нечасті, від ≥1/10000 до ˂1/1000 – поодинокі; частота невідома (не може бути оцінена за наявними даними)). У межах кожної групи за частотою виникнення побічні реакції наведені в порядку зменшення їхньої серйозності.
Найвища частота виникнення побічних реакцій, зафіксована серед різних показань, була включена у таблицю нижче. Зірочка (*) у стовпці «Органи і системи організму» вказує на наявність додаткової інформації в розділах «Протипоказання», «Особливості застосування» та «Побічні реакції».
Таблиця 7
|
Органи і системи організму |
Частота |
Побічні реакції |
|
Інфекції та інвазії* |
дуже часті |
інфекції дихальних шляхів (включаючи інфекції нижніх та верхніх відділів дихальних шляхів, пневмонію, синусит, фарингіт, ринофарингіт, пневмонію, спричинену вірусом герпесу); |
|
часті |
системні інфекції (включаючи сепсис, кандидоз та грип), кишкові інфекції (включаючи вірусний гастроентерит), інфекції шкіри та м’яких тканин (пароніхія, целюліт, імпетиго, некротичний фасциїт, оперізуючий герпес), інфекції вуха, інфекції ротової порожнини (включаючи вірус простого герпесу, герпес ротової порожнини та інфекції зубів), інфекції статевих органів (включаючи грибковий вульвовагініт), інфекції сечовивідних шляхів (включаючи пієлонефрит), грибкові інфекції, інфекції суглобів; |
|
|
нечасті |
неврологічні інфекції (включаючи вірусний менінгіт), опортуністичні інфекції та туберкульоз (включаючи кокцидіоїдомікоз, гістоплазмоз та інфекції комплексу mycobacterium avium), бактеріальні інфекції, інфекції ока, дивертикуліт1 |
|
|
Доброякісні, злоякісні та неспецифічні новоутворення (включаючи кісти та поліпи)* |
часті |
рак шкіри, за винятком меланоми (включаючи базальноклітинну карциному та плоскоклітинну карциному); доброякісні новоутворення; |
|
нечасті |
лімфома**, новоутворення паренхіматозних органів (включаючи рак молочної залози, пухлину легенів та пухлину щитовидної залози), меланома**; |
|
|
поодинокі |
лейкоз1; |
|
|
частота невідома |
гепатолієнальна Т-клітинна лімфома1, карцинома Меркеля (нейроендокринна карцинома шкіри)1 , саркома Капоші |
|
|
Порушення з боку кровоносної та лімфатичної систем* |
дуже часті |
лейкопенія (включаючи нейтропенію та агранулоцитоз), анемія; |
|
часті |
лейкоцитоз, тромбоцитопенія; |
|
|
нечасті |
ідіопатична тромбоцитопенічна пурпура; |
|
|
поодинокі |
панцитопенія |
|
|
Порушення з боку імунної системи* |
часті |
гіперчутливість, алергія (включаючи сезонну алергію); |
|
нечасті |
саркоїдоз1, васкуліт; |
|
|
поодинокі |
анафілаксія1 |
|
|
Порушення обміну речовин, метаболізму |
дуже часті |
підвищення рівня ліпідів крові; |
|
часті |
гіпокаліємія, гіперурикемія, відхилення від норми концентрації натрію у плазмі крові, гіпокальціємія, гіперглікемія, гіпофосфатемія, дегідратація |
|
|
Психічні розлади |
часті |
зміни настрою (включаючи депресію), тривога, безсоння |
|
Неврологічні розлади* |
дуже часті |
головний біль; |
|
часті |
парестезія (включаючи гіпестезію), мігрень, стиснення нервових корінців; |
|
|
нечасті |
інсульт1, тремор, невропатія; |
|
|
поодинокі |
розсіяний склероз, демієлінізуючі розлади (наприклад, неврит зорового нерва, синдром Гійєна – Барре)1 |
|
|
Порушення з боку органів зору |
часті |
порушення гостроти зору, кон’юнктивіт, блефарит, набряк ока; |
|
нечасті |
диплопія |
|
|
Порушення з боку органів слуху та вестибулярного апарату |
часті нечасті |
вертиго; глухота, дзвін у вухах |
|
Кардіальні порушення* |
часті |
тахікардія; |
|
нечасті |
інфаркт міокарда1, аритмія, хронічна серцева недостатність; |
|
|
поодинокі |
зупинка серця |
|
|
Судинні розлади |
часті |
артеріальна гіпертензія, припливи, гематома; |
|
нечасті |
аневризма аорти, оклюзія артерій, тромбофлебіт |
|
|
Порушення з боку дихальної системи, органів грудної клітки та середостіння* |
часті |
астма, диспное, кашель; |
|
нечасті |
легенева емболія1, хронічне обструктивне захворювання легенів, інтерстиціальне захворювання легенів, пневмоніт, плевральний випіт1; |
|
|
поодинокі |
легеневий фіброз1 |
|
|
Шлунково-кишкові розлади |
дуже часті |
біль у животі, нудота та блювання; |
|
часті |
шлунково-кишкова кровотеча, диспепсія, гастроезофагеальний рефлюкс, сухий синдром (синдром Шегрена); |
|
|
нечасті |
панкреатит, дисфагія, набряк обличчя; |
|
|
поодинокі |
перфорація кишечнику1 |
|
|
Розлади гепатобіліарної системи* |
дуже часті |
підвищення рівня печінкових ферментів; |
|
нечасті |
холецистит та холелітіаз, підвищення рівня білірубіну, стеатоз печінки; |
|
|
поодинокі |
гепатит, реактивація гепатиту В1, аутоімунний гепатит1; |
|
|
частота невідома |
печінкова недостатність1 |
|
|
Зміни з боку шкіри і підшкірної клітковини |
дуже часті |
висип (включаючи ексфоліативний висип); |
|
часті |
нові випадки або погіршення перебігу псоріазу (у тому числі долонно-підошовного пустульозного псоріазу)1, свербіж, кропив’янка, екхімози (включаючи пурпуру), дерматит (включаючи екзему), оніхоклазія, підвищена пітливість, алопеція1; |
|
|
нечасті |
нічна пітливість, рубці; |
|
|
поодинокі |
мультиформна еритема1, синдром Стівенса – Джонсона1, ангіоневротичний набряк1, шкірний васкуліт1, ліхеноїдна реакція шкіри1; |
|
|
частота невідома |
погіршення симптомів дерматоміозиту1 |
|
|
Порушення з боку опорно-рухової системи та сполучної тканини |
дуже часті |
скелетно-м’язовий біль; |
|
часті |
спазми м’язів (включаючи підвищення рівня креатинфосфокінази у плазмі крові); |
|
|
нечасті |
рабдоміоліз, системний червоний вовчак; |
|
|
поодинокі |
вовчакоподібний синдром 1 |
|
|
Розлади з боку сечовидільної системи |
часті |
гематурія, ниркова недостатність; |
|
нечасті |
ніктурія |
|
|
Розлади з боку репродуктивної системи та молочних залоз |
нечасті |
еректильна дисфункція |
|
Загальні розлади та реакції у місці введення* |
дуже часті |
реакції у місці введення (включаючи почервоніння у місці введення); |
|
часті |
біль у грудях, набряк, пірексія1; |
|
|
нечасті |
запалення |
|
|
Лабораторні дослідження* |
часті частота невідома |
коагуляція та порушення системи згортання крові (включаючи подовження активованого частково тромбопластинового часу (АЧТЧ)), позитивні тести на аутоантитіла (включаючи антитіла до дволанцюгової ДНК), підвищення рівня лактатдегідрогенази у плазмі крові; збільшення маси тіла2 |
|
Пошкодження, отруєння та процедурні ускладнення* |
часті |
повільне загоювання |
* Див. також розділи «Протипоказання», «Особливості застосування», «Побічні реакції».
** Включаючи відкритий період досліджень.
1 Включаючи дані спонтанних повідомлень.
2 Середня зміна маси тіла від вихідного рівня коливалася від 0,3 кг до 1,0 кг при застосуванні адалімумабу за показаннями для дорослих порівняно з (мінус) -0,4 кг до 0,4 кг при застосуванні плацебо протягом періоду лікування 4–6 місяців. Збільшення маси тіла на 5–6 кг також спостерігався у довгостроковому розширеному дослідженні із середньою експозицією приблизно 1–2 роки без контрольної групи, особливо в пацієнтів із хворобою Крона та виразковим колітом. Механізм цього ефекту незрозумілий, але може бути пов’язаний з протизапальною дією адалімумабу.
Гнійний гідраденіт
Профіль безпеки для пацієнтів із ГГ, що отримували лікування адалімумабом щотижня, відповідає відомому профілю безпеки адалімумабу.
Увеїт
Профіль безпеки для пацієнтів з увеїтом, які отримували адалімумаб 1 раз на 2 тижні, відповідає відомому профілю безпеки адалімумабу.
Опис окремих побічних реакцій
Реакції у місці введення
У контрольованих клінічних дослідженнях у дорослих та дітей, які отримували адалімумаб, у 12,9 % випадків розвинулися реакції у місці введення (еритема та/або свербіж, крововилив, біль або набряк) порівняно з 7,2 % пацієнтів контрольної групи. Більшість реакцій були легкими та загалом не потребували відміни препарату.
Інфекції
У контрольованих клінічних дослідженнях у дорослих та дітей рівень інфекцій становив 1,51/пацієнто-рік у групі пацієнтів, які отримували адалімумаб, та 1,46/пацієнто-рік у контрольній групі пацієнтів. Рівень серйозних інфекцій становив 0,04/пацієнто-рік у групі пацієнтів, які отримували адалімумаб, та 0,03/пацієнто-рік у контрольній групі пацієнтів. Переважно це були назофарингіт, інфекції верхніх дихальних шляхів та синусит. Більшість пацієнтів продовжили застосовувати адалімумаб після одужання.
У контрольованих та відкритих дослідженнях у дорослих та дітей повідомлялося про розвиток тяжких інфекцій (з летальним наслідком у поодиноких випадках): туберкульозу (у тому числі міліарного та позалегеневої локалізації) та інвазивних опортуністичних інфекцій (таких як дисемінований гістоплазмоз, пневмоцистна пневмонія, аспергільоз, лістеріоз). Більшість випадків захворювання на туберкульоз зафіксовано протягом перших восьми місяців після початку терапії і може відображати рецидив прихованої хвороби.
Новоутворення та лімфопроліферативні розлади
Протягом клінічних досліджень адалімумабу у дітей з ЮРА (поліартикулярним артритом та ентезитасоційованим артритом) злоякісні новоутворення не спостерігалося (n = 249, 655,6 пацієнто-року).
Додатково не спостерігалося злоякісних новоутворень у клінічних дослідженнях у дітей з хворобою Крона (n = 192; 498,1 пацієнто-року), бляшковим псоріазом (n = 77; 80,0 пацієнто-року), увеїтом (n = 60; 58,4 пацієнто-року).
Під час контрольованих періодів основних досліджень застосування адалімумабу дорослим протягом щонайменше 12 тижнів у пацієнтів з ревматоїдним артритом від середнього до високого ступеня активності, пацієнтів із псоріатичним артритом, аксіальним спондилоартритом (анкілозуючим спондилітом та нерентгенографічним аксіальним спондилоартритом), хворобою Крона, виразковим колітом, гнійним гідраденітом, увеїтом та псоріазом рівень новоутворень (за винятком лімфоми та немеланомного раку шкіри) становив (95 % довірчий інтервал) 6,8 (4,4; 10,5) на 1000 пацієнто-років у 5291 пацієнта, які приймали адалімумаб, в порівнянні з рівнем 6,3 (3,4; 11,8) на 1000 пацієнто-років у 3444 пацієнтів контрольної групи (середня тривалість лікування становила 4,0 місяця у групі застосування адалімумабу та 3,8 місяця у пацієнтів контрольної групи). Рівень немеланомного раку шкіри (95 % довірчий інтервал) становив 8,8 (6,0; 13,0) на 1000 пацієнто-років у пацієнтів, які приймали адалімумаб, та 3,2 (1,3; 7,6) на 1000 пацієнто-років у пацієнтів контрольної групи. Серед наведених випадків частота виникнення раку шкіри, плоскоклітинної карциноми (95 % довірчий інтервал) становила 2,7 (1,4; 5,4) на 1000 пацієнто-років у пацієнтів, які приймали адалімумаб, та 0,6 (0,1; 4,5) на 1000 пацієнто-років у пацієнтів контрольної групи. Рівень лімфом (95 % довірчий інтервал) становив 0,7 (0,2; 2,7) на 1000 пацієнто-років у пацієнтів, які приймали адалімумаб, та 0,6 (0,1; 4,5) на 1000 пацієнто-років у пацієнтів контрольної групи.
Темпи розвитку новоутворень, що спостерігалися (за винятком лімфоми та немеланомного раку шкіри), становлять приблизно 8,5/1000 пацієнто-років у контрольованих дослідженнях та у дослідженнях відкритого періоду, які ще тривають та вже завершені. Темпи розвитку немеланомного раку шкіри становили приблизно 9,6/1000 пацієнто-років, а темпи розвитку лімфом – приблизно 1,3/1000 пацієнто-років. Ці дослідження тривали приблизно 3,3 року та включали 6427 пацієнтів, які отримували адалімумаб принаймні протягом 1 року або в яких новоутворення виникли упродовж року від початку терапії, що становить більш ніж 26439 пацієнто-років терапії.
У постмаркетинговий період із січня 2003 року по грудень 2010 року переважно у пацієнтів з ревматоїдним артритом, які лікувалися адалімумабом, рівень злоякісних новоутворень становив приблизно 2,7 на 1000 пацієнто-років. Зафіксовано рівні немеланомного раку шкіри та лімфом приблизно 0,2 та 0,3 на 1000 пацієнто-років відповідно (див. розділ «Особливості застосування»).
У постмаркетинговій практиці у поодиноких випадках у пацієнтів, які застосовували адалімумаб, повідомлялося про розвиток гепатолієнальної Т-клітинної лімфоми (див. розділ «Особливості застосування»).
Аутоантитіла
У ході клінічних досліджень ревматоїдного артриту 1–5 фази пацієнтам декілька разів проводили аналіз крові на наявність аутоантитіл. У цих контрольованих дослідженнях у 11,9 % пацієнтів, які приймали адалімумаб, та у 8,1 % пацієнтів групи плацебо повідомлялося про позитивні титри, при активному моніторингу лікування спостерігалися негативні титри антинуклеарних антитіл на 24 тижні. У двох пацієнтів (із 3441 пацієнтів з РА, ПсА та АС, які отримували адалімумаб протягом клінічних випробувань) розвинулися ознаки вовчакоподібного синдрому (вперше виявленого), що зникли після припинення лікування. У жодного пацієнта не розвинулися люпус-нефрит або ураження центральної нервової системи.
Активність печінкових ферментів
У контрольованих клінічних дослідженнях 3 фази за участю пацієнтів з ревматоїдним артритом та псоріатичним артритом протягом контрольованого періоду тривалістю від 4 до 104 тижнів підвищення АЛТ (аланінтрансаміназа) у 3 або більше разів від верхньої межі норми спостерігалося у 3,7 % пацієнтів, які отримували адалімумаб, та у 1,6 % пацієнтів контрольної групи.
У контрольованих клінічних дослідженнях 3 фази за участю пацієнтів віком 4–17 років з поліартикулярним артритом та пацієнтів віком 6–17 років з ентезитасоційованим артритом підвищення АЛТ у 3 або більше разів від верхньої межі норми спостерігалося у 6,1 % пацієнтів, які отримували адалімумаб, і 1,3 % пацієнтів контрольної групи. Більшість випадків підвищення АЛТ спостерігалося під час супутньої терапії метотрексатом. Не спостерігалось підвищення АЛТ у 3 або більше разів від верхньої межі норми у клінічних дослідженнях 3 фази у пацієнтів з поліартикулярним артритом віком 2–4 роки.
У контрольованих клінічних дослідженнях 3 фази за участю пацієнтів із хворобою Крона та виразковим колітом з тривалістю контрольованого періоду від 4 до 52 тижнів підвищення АЛТ у 3 або більше разів від верхньої межі норми спостерігалося у 0,9 % пацієнтів обох груп.
У клінічному дослідженні 3 фази за участю дітей з хворобою Крона, де було оцінено ефективність та безпеку двократного відносно маси тіла режиму дозування з подальшим приведенням до режиму дозування відповідно до маси тіла з тривалістю терапії до 52 тижнів, підвищення АЛТ в 3 або більше разів вище верхньої межі норми спостерігалось у 2,6 % (5/192) пацієнтів, 4 з яких отримували адалімумаб на тлі одночасного застосування імуносупресантів.
У контрольованих клінічних дослідженнях 3 фази за участю пацієнтів з бляшковим псоріазом з тривалістю контрольного періоду від 12 до 24 тижнів підвищення АЛТ у 3 або більше разів від верхньої межі норми спостерігалося у 1,8 % пацієнтів обох груп.
У контрольованих клінічних дослідженнях (початкова доза 160 мг (тиждень 0) і 80 мг (тиждень 2), а потім 40 мг 1 раз на тиждень починаючи з тижня 4) за участю пацієнтів з гнійним гідраденітом з тривалістю контрольованого періоду від 12 до 16 тижнів підвищення АЛТ у 3 або більше разів від верхньої межі норми спостерігалося у 0,3 % пацієнтів, які отримували адалімумаб, та у 0,6 % пацієнтів контрольної групи.
У контрольованих клінічних дослідженнях (початкова доза 80 мг (тиждень 0), а потім, починаючи з тижня 1, по 40 мг 1 раз на 2 тижні) за участю пацієнтів з увеїтом з тривалістю контрольного періоду до 80 тижнів (представлені середні значення 166,5 дня та 105 днів у групі терапії адалімумабом та контрольній групі відповідно) підвищення АЛТ у 3 або більше разів від верхньої межі норми спостерігалося у 2,4 % пацієнтів, які отримували адалімумаб, та у 2,4 % пацієнтів контрольної групи.
У контрольованому дослідженні 3 фази застосування адалімумабу дітям з виразковим колітом (N = 93), в якому оцінювали ефективність та безпеку застосування підтримуючої дози 0,6 мг/кг (максимум 40 мг) при введенні один раз на 2 тижні (N = 31) та підтримуючої дози 0,6 мг/кг (максимум 40 мг) при введенні щотижня (N = 32) після застосування індукційної дози залежно від маси тіла 2,4 мг/кг (максимум 160 мг) на тижні 0 і тижні 1 та дози 1,2 мг/кг (максимум 80 мг) на тижні 2 (N = 63) або після застосування індукційної дози 2,4 мг/кг (максимум 160 мг) на тижні 0, плацебо на тижні 1 та дози 1,2 мг/кг (максимум 80 мг) на тижні 2 (N = 30), випадки підвищення активності АЛТ у 3 або більше разів від верхньої межі норми спостерігались у 1,1 % (1/93) пацієнтів.
При застосуванні за всіма показаннями у клінічних випробуваннях пацієнти мали безсимптомне підвищення рівня АЛТ і в більшості випадків підвищення було минущим на тлі тривалого лікування. Однак були дуже рідкісні постмаркетингові повідомлення про печінкову недостатність та менш серйозні печінкові реакції, що можуть призвести до печінкової недостатності, такі як гепатит, включаючи аутоімунний гепатит, у хворих, які отримували адалімумаб.
Супутня терапія з азатіоприном/6-меркаптопурином
У дослідженнях у дорослих пацієнтів з хворобою Крона, які отримували адалімумаб у комбінації з азатіоприном/6-меркаптопурином, спостерігалося підвищення частоти виникнення новоутворень та тяжких інфекцій порівняно з пацієнтами, які отримували монотерапію адалімумабом.
Повідомлення про побічні реакції після реєстрації лікарського засобу має важливе значення. Це дає змогу проводити моніторинг співвідношення користь/ризик при застосуванні цього лікарського засобу. Медичним та фармацевтичним працівникам, а також пацієнтам або їхнім законним представникам слід повідомляти про усі випадки підозрюваних побічних реакцій та відсутності ефективності лікарського засобу через Автоматизовану інформаційну систему з фармаконагляду за посиланням: https://aisf.dec.gov.ua.
Термін придатності. 2 роки.
Не слід застосовувати препарат після закінчення терміну придатності.
Умови зберігання
Зберігати при температурі 2–8 °С в оригінальній упаковці для захисту від світла. Не заморожувати. Зберігати у недоступному для дітей місці.
Дозволяється зберігати попередньо наповнений шприц при температурі не вище 25 °C протягом не більше 42 діб. Попередньо наповнений шприц слід зберігати у захищеному від світла місці та утилізувати, якщо він не був використаний протягом 42 діб.
Несумісність
У зв’язку з тим, що дослідження сумісності цього лікарського засобу не проводилися, його не можна змішувати з іншими лікарськими засобами.
Упаковка
По 20 мг / 0,2 мл розчину в попередньо наповненому шприці; по 2 попередньо наповнених шприців у блістерах у картонній коробці.
Категорія відпуску. За рецептом.
Виробник
Новартіс Фармасьютікал Мануфактурінг ГмбХ
або
Сандоз ГмбХ – Виробнича дільниця Асептичні лікарські засоби Шафтенау (Асептичні ЛЗШ)
Місцезнаходження виробника та адреса місця провадження його діяльності
Біохеміштрассе 10, Унтерлангкампфен, Лангкампфен, 6336, Австрія
або
Біохеміштрассе 10, 6336 Лангкампфен, Австрія
ІНСТРУКЦІЯ
для медичного застосування лікарського засобу
Хайрімоз
(Hyrimoz)
Склад:
діюча речовина: адалімумаб;
1 попередньо наповнений шприц містить 40 мг адалімумабу у 0,4 мл розчину;
допоміжні речовини: кислота адипінова; маніт (Е 421); полісорбат 80; натрію гідроксид (для коригування рН); кислота хлористоводнева (для коригування рН); вода для ін’єкцій.
Лікарська форма. Розчин для ін’єкцій.
Основні фізико-хімічні властивості: прозорий або дещо опалесцюючий, безбарвний або злегка жовтуватий розчин.
Фармакотерапевтична група
Імуносупресанти. Інгібітори фактора некрозу пухлини-альфа. Адалімумаб.
Код АТХ L04А В04.
Фармакологічні властивості
Механізм дії
Адалімумаб специфічно зв’язується з фактором некрозу пухлин (ФНП) та нейтралізує біологічні ефекти ФНП, блокуючи його взаємодію з p55- та p75-рецепторами ФНП на поверхні клітини.
Адалімумаб модулює також біологічні реакції відповіді, що індукуються або регулюються ФНП, включаючи зміни рівнів молекул адгезії, відповідальних за міграцію лейкоцитів (ELAM-1, VCAM-1 та ICAM-1 при IC50 0,1–0,2 нМ).
Фармакодинаміка
У пацієнтів з ревматоїдним артритом (РА) адалімумаб спричиняв швидке зменшення, порівняно з початковими параметрами, показників гострої фази запалення (С-реактивного протеїну (СРП), цитокінів сироватки крові (IL-6) та швидкості осідання еритроцитів (ШОЕ)) у пацієнтів з ревматоїдним артритом. Також спостерігалося зниження рівнів матриксних металопротеїназ (MMP-1 та MMP-3) у сироватці крові, які спричиняють ремоделювання тканин, що лежить в основі руйнування хряща. При застосуванні адалімумабу зазвичай спостерігається покращення гематологічних ознак хронічного запалення.
Після лікування адалімумабом швидке зниження рівнів СРП спостерігалося також і у пацієнтів з поліартикулярним ювенільним ідіопатичним артритом (ЮІА), хворобою Крона (ХК), виразковим колітом (ВК) та гнійним гідраденітом (ГГ). Водночас зі значущим зменшенням експресії ФНП-α у пацієнтів з хворобою Крона спостерігалося зменшення кількості клітин, що експресують запальні маркери в товстій кишці. Ендоскопічні дослідження слизової оболонки кишечнику пацієнтів, які отримували адалімумаб, продемонстрували ознаки загоєння.
Фармакокінетика
Абсорбція та розподіл
Після одноразового підшкірного введення 40 мг адалімумабу абсорбція та розподіл адалімумабу були повільними, середня пікова концентрація в сироватці крові досягалася приблизно через 5 днів після введення. Середня абсолютна біодоступність адалімумабу, розрахована в трьох дослідженнях, після застосування одноразової дози 40 мг підшкірно становила 64 %.
Після одноразового внутрішньовенного введення у дозах від 0,25 до 10 мг/кг концентрації були пропорційні дозам. Після застосування дози 0,5 мг/кг (приблизно 40 мг) кліренс був у діапазоні 11–15 мл/год, об’єм розподілу (Vss) становив від 5 до 6 л, середній термінальний період напіввиведення становив приблизно 2 тижні. Концентрації адалімумабу у синовіальній рідині у пацієнтів з РА становили 31–96 % від рівня в сироватці крові.
Після підшкірного застосування адалімумабу у дозі 40 мг 1 раз на 2 тижні у пацієнтів з РА рівноважні концентрації становили від 5 мкг/мл (без супутнього застосування метотрексату) до 8–9 мкг/мл (з метотрексатом) відповідно. Концентрації адалімумабу в сироватці крові у рівноважному стані зростали майже пропорційно до підшкірно введених доз 20, 40 та 80 мг 1 раз на 2 тижні або щотижня.
Після підшкірного застосування адалімумабу у дозі 24 мг/м2 (до 40 мг) 1 раз на 2 тижні у пацієнтів з поліартикулярним ювенільним ревматоїдним артритом (ЮРА) віком від 4 до 17 років рівноважні концентрації (показники вимірювались з 20-го по 48-й тиждень) становили 5,6 ± 5,6 мкг/мл (102 % CV – коефіцієнт варіації) без супутнього застосування метотрексату та 10,9 ± 5,2 мкг/мл (47,7 % CV) – з метотрексатом.
У дітей з поліартикулярним ЮРА віком 2–4 роки та у дітей віком від 4 років, маса тіла яких менше 15 кг, після застосування адалімумабу у дозі 24 мг/м2 з метотрексатом середнє значення рівноважних концентрацій становило 6,0 ± 6,1 мкг/мл (101 % CV) без супутнього застосування метотрексату та 7,9 ± 5,6 мкг/мл (71,2 % CV) – з метотрексатом.
Після підшкірного застосування адалімумабу у дозі 24 мг/м2 (до 40 мг) 1 раз на 2 тижні у пацієнтів віком від 6 до 17 років з ентезитасоційованим артритом рівноважні концентрації (показники вимірювались на 24-му тижні) становили 8,8 ± 6,6 мкг/мл без супутнього застосування метотрексату та 11,8 ± 4,3 мкг/мл – з метотрексатом.
Після підшкірного застосування адалімумабу в дозі 40 мг 1 раз на 2 тижні дорослим пацієнтам з нерентгенологічним аксіальним спондилоартритом середня (± стандартне відхилення) рівноважна концентрація на тижні 68 становила 8,0 ± 4,6 мкг/мл.
У дорослих пацієнтів із псоріазом середня рівноважна концентрація становила 5 мкг/мл протягом монотерапії адалімумабом у дозі 40 мг 1 раз на 2 тижні.
Після підшкірного застосування адалімумабу у дозі 0,8 мг/кг (до максимум 40 мг) 1 раз на 2 тижні у дітей із хронічним бляшковим псоріазом рівноважні концентрації становили приблизно 7,4 ± 5,8 мкг/мл (79 % CV).
У пацієнтів з гнійним гідраденітом після введення адалімумабу у дозі 160 мг на тижні 0 з наступним введенням 80 мг на тижні 2 його концентрація у сироватці крові становила приблизно від 7 до 8 мкг/мл на тижні 2 та тижні 4. Середня рівноважна концентрація з тижня 12 до тижня 36 становила приблизно від 8 до 10 мкг/мл під час введення адалімумабу у дозі 40 мг кожного тижня.
Вплив адалімумабу на підлітків з гідраденітом було визначено за допомогою фармакокінетичного моделювання та симуляції на основі фармакокінетики при інших показаннях у дітей (бляшковий псоріаз, ювенільний ревматоїдний (ідіопатичний) артрит (ЮРА), хвороба Крона (ХК) та ентезитасоційований артрит). Рекомендований режим дозування для підлітків з гідраденітом – 40 мг 1 раз на 2 тижні. Оскільки вплив адалімумабу може залежати від маси тіла, підліткам з високою масою тіла та недостатньою відповіддю на лікування можна застосовувати рекомендовану дозу для дорослих – по 40 мг 1 раз на тиждень.
У пацієнтів з хворобою Крона після введення адалімумабу у дозі 80 мг на тижні 0 з наступним введенням 40 мг на тижні 2 концентрація у сироватці крові становила приблизно 5,5 мкг/мл протягом індукційної терапії. Після введення адалімумаба у дозі 160 мг на тижні 0 з наступним введенням 80 мг на тижні 2 його концентрація у сироватці крові становила приблизно 12 мкг/мл протягом індукційної терапії. Середня рівноважна концентрація становила приблизно 7 мкг/мл під час введення адалімумабу у підтримуючій дозі 40 мг 1 раз на 2 тижні.
У дітей з хворобою Крона середнього та високого ступеня активності початкова доза адалімумабу у відкритому дослідженні становила 160/80 мг або 80/40 мг на тижнях 0 та 2 залежно від маси тіла. На тижні 4 пацієнти були рандомізовані в співвідношенні 1 : 1 у групи, які отримували залежно від маси тіла або стандартну дозу (40/20 мг 1 раз на 2 тижні), або низьку дозу (20/10 мг 1 раз на 2 тижні) для підтримуючої терапії. Середня рівноважна концентрація становила приблизно 15,7 ± 6,6 мкг/мл на тижні 4 у пацієнтів з масою тіла 40 кг або більше (160/80 мг) та 10,6 ± 6,1 мкг/мл у пацієнтів з масою тіла менше 40 кг (80/40 кг).
У пацієнтів, які продовжували лікування в своїй групі, середні (± стандартне відхилення) концентрації адалімумабу на тижні 52 становили 9,5 ± 5,6 мкг/мл у групі стандартних доз та 3,5 ± 2,2 мкг/мл у групі низьких доз. Середні концентрації зберігалися у пацієнтів, які продовжували отримувати лікування адалімумабом протягом 52 тижнів. Для пацієнтів, яким дозу збільшили з однієї 1 раз на два тижні до однієї щотижня, середні (± стандартне відхилення) концентрації адалімумабу в сироватці крові на тижні 52 становили 15,3 ± 11,4 мкг/мл (40/20 мг, щотижня) та 6,7 ± 3,5 мкг/мл (20/10 мг, щотижня).
У пацієнтів з виразковим колітом після введення адалімумабу у початковій дозі 160 мг на тижні 0 з наступним введенням 80 мг на тижні 2 його концентрація у сироватці крові становила приблизно 12 мкг/мл протягом індукційної терапії. Середня рівноважна концентрація становила приблизно 8 мкг/мл під час введення адалімумабу у підтримуючій дозі 40 мг 1 раз на 2 тижні.
У дітей з виразковим колітом середня рівноважна концентрація адалімумабу у сироватці крові на тижні 52 після підшкірного введення дози залежно від маси тіла 0,6 мг/кг (максимум 40 мг) один раз на два тижні становила 5,01 ± 3,28 мкг/мл. У пацієнтів, яким вводили дозу 0,6 мг/кг (максимум 40 мг) кожного тижня, середня (± стандартне відхилення) рівноважна концентрація адалімумабу в сироватці крові на тижні 52 становила 15,7 ± 5,60 мкг/мл.
У дорослих пацієнтів з увеїтом після введення адалімумабу у початковій дозі 80 мг на тижні 0 з наступним введенням 40 мг 1 раз на 2 тижні, починаючи з тижня 1, середня рівноважна концентрація становила приблизно від 8 до 10 мкг/мл.
Вплив адалімумабу на стан дітей з увеїтом було визначено за допомогою фармакокінетичного моделювання та симуляції на основі фармакокінетики при інших показаннях у дітей (бляшковий псоріаз, ювенільний ревматоїдний (ідіопатичний) артрит (ЮРА), хвороба Крона (ХК) та ентезитасоційований артрит). Немає клінічних даних про вплив початкової дози адалімумабу на стан дітей віком до 6 років. Прогнозується, що за відсутності метотрексату початкова доза може призвести до підвищення системного впливу.
Популяційне фармакокінетичне та фармакокінетичне/фармакодинамічне моделювання і симуляція передбачили порівнянний вплив та ефективність адалімумабу в пацієнтів, які отримували 80 мг 1 раз на 2 тижні, та у пацієнтів, які отримували щотижнево дозу 40 мг (включаючи дорослих пацієнтів з РА, ГГ, ВК, ХК або псоріазом, дітей з ГГ та дітей масою тіла 40 кг і більше з ХК та ВК).
Залежність «вплив – відповідь» у дітей
На основі даних клінічних досліджень у пацієнтів з ЮІА (поліартикулярний ювенільний ідіопатичний артрит та ентезитасоційований артрит) було встановлено залежність «вплив – відповідь» між концентрацією в плазмі крові та відповіддю за критерієм PedACR 50. Очевидна концентрація адалімумабу в плазмі крові, яка забезпечує половину максимальної ймовірності відповіді PedACR 50 (EC50), становила 3 мкг/мл (95 % ДІ 1–6 мкг/мл). Залежність «вплив – відповідь» між концентрацією адалімумабу та його ефективністю у дітей з хронічним бляшковим псоріазом високого ступеня тяжкості була встановлена для відповідей за індексом PASI 75 та PGA («відсутність» або «мінімальний» відповідно). Показники PASI 75 та PGA «відсутність» або «мінімальний» зростали зі збільшенням концентрації адалімумабу, при цьому обидва показники мали подібну явну EC50 приблизно 4,5 мкг/мл (95 % ДІ 0,4–47,6 та 1,9–10,5 відповідно).
Виведення
Популяційний фармакокінетичний аналіз даних більше ніж 1300 пацієнтів з РА виявив тенденцію до підвищення явного кліренсу адалімумабу з підвищенням маси тіла пацієнтів. З урахуванням поправок щодо різниці маси тіла було встановлено, що стать та вік пацієнта мають мінімальний вплив на кліренс адалімумабу. Рівні вільного адалімумабу (не зв’язаного з антитілами до адалімумабу в сироватці крові були нижчими у пацієнтів, у яких виявлялись антитіла до адалімумабу. Не вивчали застосування лікарського засобу Хайрімоз пацієнтам із порушеннями функцій печінки та нирок.
Клінічні характеристики
Показання
Ревматоїдний артрит (РА)
Хайрімоз у комбінації з метотрексатом показаний для:
· лікування ревматоїдного артриту середнього та високого ступеня активності у дорослих пацієнтів, коли адекватна відповідь на терапію протиревматичними препаратами, що модифікують перебіг захворювання (DMARDs – disease-modifying antirheumatic drugs), включаючи метотрексат, не була отримана;
· лікування активного прогресуючого ревматоїдного артриту високого ступеня активності у дорослих пацієнтів, які раніше не отримували терапію метотрексатом.
Хайрімоз можна застосовувати як монотерапію у разі непереносимості метотрексату або коли продовження терапії метотрексатом є неприйнятним.
Адалімумаб продемонстрував пригнічення прогресування структурного ураження суглобів, що було підтверджено рентгенографічно, та покращення функціонального стану при одночасному застосуванні з метотрексатом.
Ювенільний ревматоїдний (ідіопатичний) артрит (ЮРА)
Поліартикулярний ювенільний ревматоїдний (ідіопатичний) артрит
Хайрімоз у комбінації з метотрексатом показаний для лікування активного поліартикулярного ювенільного ідіопатичного артриту у дітей віком від 2 років, у яких не було адекватної відповіді на терапію одним або кількома протиревматичними препаратами, що модифікують перебіг захворювання (DMARDs).
Хайрімоз можна застосовувати як монотерапію у разі непереносимості метотрексату або коли продовження терапії метотрексатом є неприйнятним. Не було проведено досліджень застосування препарату Хайрімоз пацієнтам віком до 2 років.
Ентезитасоційований артрит
Хайрімоз показаний для лікування активного ентезитасоційованого артриту у дітей віком від 6 років, які не відповідали на традиційну терапію або мають непереносимість чи медичні протипоказання до таких видів терапії.
Аксіальний спондилоартрит
Анкілозуючий спондиліт (АС)
Хайрімоз показаний для лікування анкілозуючого спондиліту з високим ступенем активності у дорослих пацієнтів, які не відповіли на традиційну терапію.
Аксіальний спондилоартрит без рентгенологічного підтвердження АС
Хайрімоз показаний для лікування аксіального спондилоартриту з високим ступенем активності без рентгенологічного підтвердження АС, але з наявними ознаками запалення на підставі підвищеного рівня СРП та/або за результатами МРТ (магнітно-резонансна томографія) у дорослих пацієнтів, у яких не було адекватної відповіді на терапію нестероїдними протизапальними препаратами (НПЗП) або наявна непереносимість цих препаратів.
Псоріатичний артрит (ПсА)
Хайрімоз показаний для лікування активного та прогресуючого псоріатичного артриту у дорослих пацієнтів, коли не було отримано адекватної відповіді на попередню терапію протиревматичними препаратами, що модифікують перебіг захворювання (DMARDs). Адалімумаб продемонстрував уповільнення темпів прогресування ураження периферичних суглобів, що визначається за допомогою рентгенографії, у пацієнтів із симетричною поліартикулярною формою захворювання та покращання функціонального стану.
Бляшковий псоріаз (БП)
Хайрімоз показаний для лікування дорослих пацієнтів із помірним або тяжким перебігом хронічного бляшкового псоріазу, яким необхідна системна терапія.
Бляшковий псоріаз (БП) у дітей
Хайрімоз показаний для лікування хронічного бляшкового псоріазу з тяжким перебігом у дітей віком від 4 років, у яких не отримано клінічної відповіді або є протипоказання/ непереносимість місцевої терапії або фототерапії.
Гнійний гідраденіт (ГГ)
Хайрімоз показаний для лікування активного помірного та тяжкого гнійного гідраденіту (acne inversa) у дорослих пацієнтів та у підлітків віком від 12 років, які не відповідали на традиційну системну терапію.
Хвороба Крона (ХК)
Хайрімоз показаний для лікування хвороби Крона середнього та високого ступеня активності у дорослих пацієнтів, які не відповідали на повний курс терапії кортикостероїдами та/або імуносупресантами або мають непереносимість чи медичні протипоказання до таких видів терапії.
Хвороба Крона (ХК) у дітей
Хайрімоз показаний для лікування хвороби Крона середнього та високого ступеня активності у дітей віком від 6 років, які не відповідали на традиційну терапію, включаючи первинну нутритивну терапію, терапію кортикостероїдами та/або імуномодуляторами, або мають непереносимість чи медичні протипоказання до таких видів терапії.
Виразковий коліт (ВК)
Хайрімоз показаний для лікування виразкового коліту середнього та високого ступеня активності у дорослих, які не відповідали на традиційну терапію, включаючи терапію кортикостероїдами та/або 6-меркаптопурином або азатіоприном, або мають непереносимість чи медичні протипоказання до таких видів терапії.
Виразковий коліт (ВК) у дітей
Хайрімоз показаний для лікування виразкового коліту середнього та високого ступеня активності у дітей віком від 6 років, які не відповідали на традиційну терапію, включаючи терапію кортикостероїдами та/або 6-меркаптопурином або азатіоприном, або мають непереносимість чи медичні протипоказання до таких видів терапії.
Увеїт
Хайрімоз показаний для лікування неінфекційного інтермедіарного, заднього та панувеїту у дорослих пацієнтів, які не відповідали на терапію кортикостероїдами, яким необхідно знизити дозу кортикостероїдів або які мають непереносимість чи медичні протипоказання до терапії кортикостероїдами.
Увеїт у дітей
Хайрімоз показаний для лікування хронічного неінфекційного переднього увеїту у дітей віком від 2 років, які не відповідали на традиційну терапію або мають непереносимість традиційної терапії або яким традиційна терапія протипоказана.
Протипоказання
· Підвищена чутливість до адалімумабу або до будь-якого іншого компонента препарату.
· Активний туберкульоз або інші тяжкі інфекції, такі як сепсис та опортуністичні інфекції (див. розділ «Особливості застосування»).
· Помірна та тяжка серцева недостатність (III/IV клас за NYHA) (див. розділ «Особливості застосування»).
Взаємодія з іншими лікарськими засобами та інші види взаємодій
Адалімумаб вивчали за участю пацієнтів з РА, ЮРА та ПсА, які отримували препарат як монотерапію та одночасно з метотрексатом. Рівень формування антитіл був нижчим при одночасному застосуванні адалімумабу з метотрексатом порівняно з монотерапією. Введення адалімумабу без метотрексату призводило до збільшення рівня формування антитіл, збільшення кліренсу та зниження ефективності адалімумабу.
· Не рекомендується одночасне застосовування препарату Хайрімоз із анакінрою (див. розділ «Особливості застосування»).
· Не рекомендується одночасне застосовування препарату Хайрімоз із абатацептом (див. розділ «Особливості застосування»).
Особливості застосування
З метою покращення контролю застосування біологічних препаратів необхідно чітко фіксувати торгівельну назву та номер серії введеного препарату у медичній документації пацієнта.
Інфекції
Пацієнти, які застосовували блокатори ФНП, більш схильні до розвитку тяжких інфекцій.
Порушення функції легенів може збільшити ризик розвитку інфекцій. Тому за станом пацієнтів слід ретельно стежити та перевіряти їх на наявність інфекцій, включаючи туберкульоз, до, під час та після лікування препаратом Хайрімоз. Оскільки елімінація адалімумабу може тривати до чотирьох місяців, спостереження слід продовжувати протягом цього періоду.
Не слід застосовувати адалімумаб пацієнтам з активним інфекційним процесом, включаючи хронічні або локалізовані інфекції, поки інфекція не буде контрольована. У пацієнтів, які мають контакт із хворим на туберкульоз або повернулися з країн з високим рівнем захворюваності на туберкульоз або з ендемічних зон щодо мікозів (гістоплазмоз, кокцидіоїдомікоз або бластомікоз), слід оцінити співвідношення користь/ризик до початку застосування препарату Хайрімоз (див. нижче «Інші опортуністичні інфекції»).
Необхідно провести повне обстеження та ретельно спостерігати за станом пацієнтів, у яких під час лікування препаратом Хайрімоз розвинулася нова інфекція. При розвитку тяжкої інфекції або сепсису слід припинити лікування та застосувати відповідні протимікробні або протигрибкові препарати, поки інфекція не буде контрольована. Слід з особливою обережністю застосовувати Хайрімоз пацієнтам з рекурентними інфекціями або при преморбідних станах, що підвищують схильність до розвитку інфекцій.
Тяжкі інфекції
Тяжкі інфекції, такі як сепсис, спричинений бактеріальними, мікобактеріальними, інвазивними грибковими, паразитарними, вірусними або іншими опортуністичними інфекціями (лістеріоз, легіонельоз і пневмоцистоз), спостерігалися у пацієнтів, які застосовували адалімумаб.
У клінічних дослідженнях спостерігалися й інші тяжкі інфекції: пневмонія, пієлонефрит, септичний артрит та септицемія. Були повідомлення про госпіталізацію пацієнтів з інфекціями, що виникли (у тому числі про летальні випадки).
Туберкульоз
Повідомлялося про випадки реактивації та про розвиток нової інфекції туберкульозу, включаючи легеневу та нелегеневу форми (тобто дисемінований туберкульоз), у пацієнтів, які отримували лікування адалімумабом. До початку терапії препаратом Хайрімоз пацієнтів потрібно ретельно обстежити щодо активного та неактивного (латентного) туберкульозу. Обстеження повинно включати вичерпну оцінку анамнезу пацієнта з туберкульозом або відомості про можливі контакти з хворими на активний туберкульоз та про попередню та/або супутню імуносупресивну терапію. Слід провести всім пацієнтам до початку терапії шкірний туберкуліновий тест (проба Манту) та рентгенографію грудної клітки (можуть застосовуватися місцеві рекомендації). Проведення та результати проб рекомендується фіксувати в картці-пам’ятці пацієнта. Лікарі повинні пам’ятати про ризик хибнонегативних результатів шкірних туберкулінових тестів, особливо у тяжкохворих пацієнтів або пацієнтів з ослабленим імунітетом.
Терапію лікарським засобом Хайрімоз не слід проводити, якщо діагностується активний туберкульоз (див. розділ «Протипоказання»).
У всіх ситуаціях, описаних нижче, слід дуже ретельно зважити співвідношення користь/ризик терапії.
Рішення про лікування пацієнтів з підозрою на латентний туберкульоз слід приймати після консультації з фтизіатром.
У разі латентного туберкульозу перед початком терапії лікарським засобом Хайрімоз потрібно провести специфічне протитуберкульозне лікування відповідно до місцевих рекомендацій.
Слід зважати на необхідність протитуберкульозного лікування перед початком терапії лікарським засобом Хайрімоз пацієнтам, які мають фактори ризику розвитку туберкульозної інфекції, але в яких отримано негативний результат тесту на латентний туберкульоз, та пацієнтам, які мали в анамнезі латентний або активний туберкульоз і для яких не може бути підтверджене відповідне лікування.
Незважаючи на профілактичне протитуберкульозне лікування, випадки реактивації туберкульозу траплялися у пацієнтів, які отримували адалімумаб. У деяких пацієнтів, які раніше перенесли успішну терапію активного туберкульозу, спостерігався повторний розвиток туберкульозу на тлі прийому адалімумабу.
Усіх пацієнтів потрібно попередити про необхідність консультації лікаря у разі появи ознак, що нагадують симптоми туберкульозу (наприклад, постійний кашель, виснаження / зменшення маси тіла, субфебрильна температура, апатія) під час або після лікування препаратом Хайрімоз.
Інші опортуністичні інфекції
Протягом лікування адалімумабом повідомлялося про розвиток опортуністичних інфекцій, у тому числі інвазивних грибкових інфекцій. Іноді такі інфекції своєчасно не діагностувалися у пацієнтів, які застосовують антагоністи ФНП, що призводило до пізнього початку лікування та іноді завершувалося летально.
У разі розвитку лихоманки, нездужання, зменшення маси тіла, підвищення пітливості, кашлю, задишки та/або інфільтратів у легенях чи інших ознак серйозного системного захворювання (з шоком або без) пацієнтам слід негайно пройти обстеження щодо виявлення інвазивної грибкової інфекції та негайно припинити застосування препарату Хайрімоз. Рішення щодо застосування емпіричної протигрибкової терапії таким хворим слід приймати після консультації з фахівцем у сфері діагностики та лікування інвазивних грибкових інфекцій.
Реактивація гепатиту В
Застосування блокаторів ФНП, включаючи адалімумаб, пов’язувалося з реактивацією вірусу гепатиту В у хронічних носіїв (тобто тих, хто мав позитивний поверхневий антиген). Іноді випадки реактивації вірусу гепатиту В були летальними. До початку застосування препарату Хайрімоз слід обстежити пацієнтів групи ризику щодо вірусу гепатиту В. У разі позитивного результату такого обстеження рішення про лікування слід приймати після консультації з гепатологом.
Слід з обережністю призначати Хайрімоз пацієнтам, які є носіями вірусу гепатиту В, а у разі призначення – ретельно спостерігати за станом таких пацієнтів щодо появи симптомів реактивації вірусу гепатиту В під час терапії та протягом декількох місяців після припинення лікування. Немає даних щодо ефективності та безпеки застосування противірусних препаратів для профілактики реактивації вірусу гепатиту В у носіїв, які отримують антагоністи ФНП для запобігання реактивації вірусу гепатиту В. При реактивації вірусу гепатиту В слід припинити терапію препаратом Хайрімоз й призначити ефективне противірусне лікування та відповідну підтримуючу терапію.
Неврологічні розлади
При застосуванні блокаторів ФНП, у тому числі адалімумабу, повідомлялося про поодинокі випадки появи або загострення клінічних симптомів та/або радіографічних ознак демієлінізуючих захворювань центральної нервової системи, включаючи розсіяний склероз, неврит зорового нерва та демієлінізуючі захворювання периферичної нервової системи, включаючи синдром Гійєна – Барре. Рекомендується ретельна оцінка переваг/ризику застосування адалімумабу для пацієнтів з демієлінізуючими розладами центральної або периферичної нервової системи. Необхідно припинити терапію препаратом Хайрімоз у разі виникнення зазначених розладів. Відомо, що існує зв’язок між інтермедіарним увеїтом та демієлінізуючими розладами центральної нервової системи. Неврологічне обстеження необхідно проводити пацієнтам з неінфекційним інтермедіарним увеїтом перед тим, як розпочати терапію лікарським засобом Хайрімоз, та регулярно протягом терапії, щоб оцінювати розвиток демієлінізуючих розладів центральної нервової системи.
Алергічні реакції
Під час клінічних досліджень виникали поодинокі серйозні алергічні реакції, пов’язані з адалімумабом. Повідомлялося про серйозні алергічні реакції, включаючи анафілаксію, після введення адалімумабу. При виникненні анафілактичної реакції або іншої серйозної алергічної реакції необхідно негайно припинити застосування препарату Хайрімоз і розпочати відповідну терапію.
Імуносупресія
Під час клінічних досліджень адалімумабу у 64 пацієнтів з РА випадків пригнічення гіперчутливості сповільненого типу, зниження рівнів імуноглобулінів або кількісних змін ефекторних Т- та В-клітин, а також NK-клітин, моноцитів/макрофагів та нейтрофілів не спостерігалося.
Злоякісні новоутворення
У контрольованих клінічних дослідженнях блокаторів ФНП частіше повідомлялося про розвиток злоякісних новоутворень у пацієнтів, які отримували ФНП-блокатор, ніж у пацієнтів контрольної групи. Однак ці випадки були поодинокими. У постмаркетинговій практиці повідомлялося про випадки лейкемії, пов’язаної із застосуванням антагоністів ФНП. Більше того, у пацієнтів з давнім високоактивним ревматоїдним артритом існує високий фоновий ризик виникнення лімфоми та лейкемії, що ускладнює оцінку ризику. З огляду на існуючі дані не можна виключати ризик розвитку лімфом, лейкемії або інших злоякісних новоутворень у пацієнтів, які лікуються антагоністами ФНП.
З постмаркетингової практики відомо про випадки злоякісних новоутворень (у тому числі летальних) у дітей та дорослих (віком до 22 років), які отримували лікування антагоністами ФНП (вік початку терапії ≤ 18 років), включаючи адалімумаб. Лімфоми становили приблизно половину цих випадків. Решту становили різні злоякісні новоутворення, в тому числі рідкісні злоякісні новоутворення, що зазвичай асоціюються з імуносупресією. Не можна виключити ризик розвитку злоякісних новоутворень у дітей, які отримують лікування антагоністами ФНП.
У постмаркетинговій практиці були поодинокі повідомлення про розвиток гепатолієнальної Т-клітинної лімфоми у пацієнтів, які застосовували адалімумаб. Це рідкісний тип лімфоми, що характеризується дуже агресивним перебігом та зазвичай є летальним. Деякі випадки утворення гепатолієнальної Т-клітинної лімфоми на тлі лікування адалімумабом спостерігалися в молодих людей, які раніше отримували терапію інфліксимабом у комбінації з азатіоприном або 6-меркаптопурином для лікування запальних захворювань кишечнику. Потенційний ризик одночасного застосування азатіоприну або 6-меркаптопурину з адалімумабом має бути ретельно оцінений. Ризик розвитку гепатолієнальної Т-клітинної лімфоми у пацієнтів, які отримують лікування препаратом Хайрімоз, виключити не можна (див. розділ «Побічні реакції»).
Досліджень щодо застосування адалімумабу пацієнтам зі злоякісними новоутвореннями в анамнезі або продовження терапії у пацієнтів, в яких розвинулося злоякісне новоутворення, не проводилося. Отже, це потрібно враховувати та з обережністю приймати рішення щодо застосування адалімумабу таким хворим (див. розділ «Побічні реакції»).
У всіх пацієнтів, особливо при інтенсивній імуносупресивній терапії в анамнезі, або у пацієнтів із псоріазом, яким проводили PUVA-терапію (псоралени з УФА), слід виключити наявність немеланомного раку шкіри до та протягом періоду застосування лікарського засобу Хайрімоз. Також повідомлялося про меланому та карциному з клітин Меркеля у пацієнтів, які отримували лікування антагоністами ФНП, включаючи адалімумаб (див. розділ «Побічні реакції»).
У пошуковому клінічному дослідженні, в якому оцінювали застосування іншого антагоніста ФНП (інфліксимаб), у пацієнтів із хронічною обструктивною хворобою легенів повідомлялося про більш часті випадки виникнення новоутворень, здебільшого у легенях, голові та на ділянці шиї, порівняно з контрольною групою. Всі пацієнти довгий час були курцями. Тому необхідно з обережністю застосовувати будь-які антагоністи ФНП пацієнтам із хронічною обструктивною хворобою легенів та пацієнтам із підвищеним ризиком виникнення новоутворень на тлі куріння.
На сьогодні невідомо, чи впливає застосування адалімумабу на ризик розвитку дисплазії або раку товстої кишки. Усі хворі на виразковий коліт, що входять до групи підвищеного ризику розвитку дисплазії або раку товстої кишки (зокрема пацієнти з довготривалим виразковим колітом або первинним склерозуючим холангітом), або ті, хто мав в анамнезі дисплазію або рак товстої кишки, повинні підлягати регулярному обстеженню щодо наявності дисплазії перед початком терапії та протягом перебігу всієї хвороби. Обстеження має включати колоноскопію та біопсію відповідно до місцевих рекомендацій.
Гематологічні розлади
При застосуванні блокаторів ФНП були поодинокі повідомлення про розвиток панцитопенії, апластичної анемії. При застосуванні адалімумабу (причинно-наслідковий зв’язок не з’ясований) повідомлялося про розвиток цитопенії (тромбоцитопенії, лейкопенії), що мала клінічне значення. Усіх пацієнтів потрібно попередити про необхідність негайної консультації лікаря при появі симптомів, притаманних захворюванням крові (таких як постійна гарячка, синці, кровотеча, блідість шкіри та слизових оболонок), на тлі застосування адалімумабу. Слід розглянути необхідність припинення застосування препарату Хайрімоз пацієнтам у разі підтвердження серйозних порушень з боку крові.
Вакцинація
Схожі реакції антитіл на стандартну 23-валентну пневмококову вакцину та тривалентну вакцину проти грипу спостерігалися в дослідженні за участю 226 дорослих пацієнтів з ревматоїдним артритом, які застосовували адалімумаб або плацебо. Відсутні дані щодо вторинної передачі інфекції живими вакцинами в пацієнтів, які отримували адалімумаб.
Для пацієнтів дитячого віку рекомендовано по можливості провести всі необхідні щеплення згідно з календарем до початку терапії препаратом Хайрімоз.
Пацієнтам під час застосування адалімумабу можна проводити вакцинацію, за винятком застосування живих вакцин. Застосування живих вакцин (наприклад вакцини БЦЖ) немовлятам, які піддавалися впливу адалімумабу внутрішньоутробно, не рекомендується протягом 5 місяців після останньої ін’єкції адалімумабу матері у період вагітності.
Хронічна серцева недостатність (ХСН)
У клінічному дослідженні з іншим антагоністом ФНП спостерігалося погіршення перебігу застійної серцевої недостатності та підвищення рівня пов’язаної з нею смертності. Також повідомлялося про випадки погіршення перебігу застійної серцевої недостатності у пацієнтів, які застосовували адалімумаб. Хайрімоз слід з обережністю застосовувати пацієнтам із серцевою недостатністю легкого ступеня тяжкості (клас I/II за класифікацією NYHA (Нью-Йоркська асоціація кардіологів)). Застосування лікарського засобу Хайрімоз протипоказане при серцевій недостатності помірного та тяжкого ступеня (див. розділ «Протипоказання»). При виникненні нових симптомів та погіршенні перебігу застійної серцевої недостатності лікування препаратом Хайрімоз слід припинити.
Аутоімунні процеси
Лікування адалімумабом може спричинити появу аутоантитіл. Вплив тривалого застосування препарату Хайрімоз на розвиток аутоімунних захворювань невідомий. При виникненні симптомів, що нагадують вовчакоподібний синдром, і виявленні антитіл до дволанцюгової ДНК подальше лікування препаратом Хайрімоз необхідно припинити (див. розділ «Побічні реакції»).
Одночасне застосування з біологічними DMARDs або з антагоністами ФНП
Спостерігалися серйозні інфекції під час клінічних досліджень супутнього застосування анакінри та етанерцепту, що не мало терапевтичних переваг у порівнянні з монотерапією етанерцептом. З огляду на характер побічних явищ, що спостерігалися під час комбінованого лікування етанерцептом та анакінрою, подібна токсичність може розвинутися при комбінації анакінри та іншого блокатора ФНП. Тому комбінація адалімумабу та анакінри не рекомендується (див. розділ «Взаємодія з іншими лікарськими засобами та інші види взаємодій»).
Одночасне застосування адалімумабу з іншими біологічними DMARDs (наприклад, анакінра та абатацепт) або з іншими антагоністами ФНП не рекомендується, зважаючи на можливе підвищення ризику інфекцій та інших потенційних фармакологічних взаємодій (див. розділ «Взаємодія з іншими лікарськими засобами та інші види взаємодій»).
Хірургічні втручання
Доступні обмежені дані щодо безпеки хірургічних процедур у пацієнтів, які отримують адалімумаб. Тривалий період напіввиведення адалімумабу необхідно брати до уваги, якщо планується хірургічне втручання. Пацієнта, який потребує хірургічного втручання та знаходиться на лікуванні препаратом Хайрімоз, потрібно ретельно обстежити на наявність інфекцій. У разі необхідності слід вжити відповідних заходів. Доступні обмежені дані щодо безпеки застосування пацієнтам, які піддавались артропластиці під час терапії адалімумабом.
Непрохідність тонкої кишки
Відсутність відповіді на лікування хвороби Крона може свідчити про наявність фіксованої фіброзної стриктури, яка вимагає лікування хірургічним шляхом. Доступні дані дають змогу вважати, що лікування адалімумабом не спричиняє виникнення або прогресування стриктур.
Пацієнти літнього віку
Частота розвитку серйозних інфекцій у пацієнтів віком від 65 років, які отримували адалімумаб (3,7 %), вища, ніж у молодших пацієнтів (1,5 %). Деякі випадки були летальними. У зв’язку з тим, що частота розвитку інфекцій у пацієнтів літнього віку вища, застосовувати адалімумаб пацієнтам цієї вікової категорії необхідно з обережністю.
Діти
Див. підрозділ «Вакцинація» вище.
Допоміжні речовини з відомими ефектами
Лікарський засіб Хайрімоз містить менше 1 ммоль (23 мг) на 0,4 мл натрію, тобто практично вільний від натрію.
Застосування у період вагітності або годування груддю
Жінки репродуктивного віку
Для запобігання вагітності жінки репродуктивного віку повинні користуватися надійними методами контрацепції під час лікування та протягом щонайменше п’яти місяців після введення останньої дози препарату Хайрімоз.
Вагітність
В результаті проспективного аналізу даних щодо застосування адалімумабу під час вагітності (приблизно 2100 випадків вагітностей, які завершилися народженням живих дітей з відомими наслідками, у тому числі понад 1500 випадків застосування препарату у першому триместрі) не виявлено збільшення частоти виникнення вад розвитку у новонароджених.
В проспективний когортний реєстр було включено 257 жінок з РА або ХК, які отримували адалімумаб як мінімум протягом першого триместру, та 120 жінок з РА або ХК, які не отримували адалімумаб. Первинною кінцевою точкою була частота розвитку значних вроджених вад у новонароджених. Частота випадків вагітностей, які завершилися народженням принаймні однієї живої дитини зі значною вродженою вадою, становила 6 з 69 (8,7 %) в групі жінок з РА, які отримували адалімумаб, та 5 з 74 (6,8 %) – в групі жінок з РА, які не застосовували препарат (нескориговане відношення шансів [ВШ] 1,31, 95 % довірчий інтервал [ДІ] 0,38–4,52). В групі жінок з ХК, які отримували адалімумаб, частота таких випадків становила 16 зі 152 (10,5 %), а в групі жінок з ХК, які не застосовували препарат, відповідно 3 з 32 (9,4 %) (нескориговане ВШ 1,14, 95 % ДІ 0,31–4,16). В об’єднаній групі жінок з РА та ХК скориговане ВШ (з поправкою на відмінності на вихідному рівні) становило 1,10 (95 % ДІ 0,45–2,73). Між жінками, які застосовували та не застосовували адалімумаб, не було виявлено чітко виражених відмінностей щодо вторинних кінцевих точок у вигляді спонтанних абортів, незначних вроджених вад, передчасних пологів, маси тіла та зросту новонароджених і серйозних або опортуністичних інфекцій, а також не було зареєстровано випадків мертвонародження або розвитку злоякісних пухлин. На інтерпретацію даних могли впливати методологічні обмеження дослідження, у тому числі малий об’єм вибірки та нерандомізований дизайн дослідження.
В експериментальному дослідженні токсичності на мавпах не було виявлено ознак токсичної дії на материнський організм, а також ембріотоксичної та тератогенної дії. Доклінічні дані щодо постнатальної токсичності адалімумабу відсутні.
Оскільки адалімумаб інгібує ФНП-α, його застосування під час вагітності може порушити нормальні імунні реакції у новонародженого. Вагітним жінкам слід застосовувати адалімумаб лише у разі очевидної необхідності.
Адалімумаб може проникати через плаценту в сироватку крові новонароджених, матері яких отримували адалімумаб під час вагітності. Тому у таких новонароджених може бути підвищений ризик інфікування. Застосування живих вакцин (наприклад вакцини БЦЖ) немовлятам, що піддавалися впливу адалімумабу внутрішньоутробно, не рекомендується протягом 5 місяців після останньої ін’єкції адалімумабу матері у період вагітності.
Годування груддю
Обмежені опубліковані дані свідчать про те, що адалімумаб екскретується у грудне молоко у дуже низьких концентраціях – від 0,1 % до 1 % від рівня у сироватці матері. Враховуючи те, що білки імуноглобуліну G піддаються в кишечнику протеолізу і мають низьку біодоступність, системний вплив адалімумабу на немовлят, які знаходяться на грудному вигодовуванні, малоймовірний. Отже, препарат Хайрімоз можна застосовувати в період годування груддю.
Фертильність
Доклінічні дані щодо впливу адалімумабу на фертильність відсутні.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами
Хайрімоз може мати незначний вплив на швидкість реакції при керуванні автотранспортом або іншими механізмами. Застосування лікарського засобу Хайрімоз може спричинити виникнення вертиго та порушення гостроти зору (див. розділ «Побічні реакції»).
Спосіб застосування та дози
Терапію препаратом Хайрімоз повинен призначати лікар, який має досвід діагностування та терапії захворювань, при яких показаний Хайрімоз. Офтальмологам рекомендовано проконсультуватися з відповідним спеціалістом перед тим, як призначати терапію препаратом Хайрімоз. Пацієнти, які застосовують лікарський засіб Хайрімоз, повинні отримати картку-пам’ятку пацієнта.
Хайрімоз можна вводити самостійно тільки у разі, якщо пацієнт або батьки дитини, якій призначена терапія адалімумабом, пройшли відповідний інструктаж у лікаря щодо техніки введення ін’єкції та лікар підтвердив, що це можливо. Додатково необхідно ознайомитись з інформацією щодо самостійного введення, яка міститься в цій інструкції. Під час лікування препаратом Хайрімоз інші супутні види терапії (наприклад терапію кортикостероїдами та/або імуномодулюючими препаратами) потрібно переглянути.
Ревматоїдний артрит
Рекомендована доза для дорослих пацієнтів становить 40 мг 1 раз на 2 тижні підшкірно. Під час терапії лікарським засобом Хайрімоз необхідно продовжувати застосовувати метотрексат, також можна продовжувати терапію глюкокортикоїдами, саліцилатами, нестероїдними протизапальними препаратами, аналгетиками. Щодо застосування інших протиревматичних препаратів, які модифікують перебіг захворювання (DMARDs), див. розділ «Особливості застосування».
Для деяких хворих на РА, які не застосовують метотрексат, може бути виправданим збільшення частоти введення препарату до 40 мг 1 раз на тиждень підшкірно або 80 мг 1 раз на 2 тижні.
Клінічна відповідь зазвичай досягається протягом 12 тижнів лікування. Слід переглянути необхідність продовження терапії для пацієнтів, у яких протягом вказаного терміну не спостерігається відповіді на лікування.
Якщо необхідно, можна перервати терапію (наприклад, перед хірургічним втручанням або у разі тяжкої інфекції). Існують дані, що після повернення до терапії через 70 днів або більше клінічна відповідь та профіль безпеки є подібними до тих, що були до перерви.
Аксіальний спондилоартрит (анкілозуючий спондиліт та аксіальний спондилоартрит без рентгенологічного підтвердження АС) та псоріатичний артрит
Рекомендована доза для дорослих пацієнтів становить 40 мг 1 раз на 2 тижні підшкірно.
Клінічна відповідь зазвичай досягається протягом 12 тижнів лікування. Слід переглянути необхідність продовження терапії для пацієнтів, у яких протягом вказаного терміну не спостерігається відповіді на лікування.
Бляшковий псоріаз
Рекомендована початкова доза для дорослих становить 80 мг, через 1 тиждень застосовувати 40 мг підшкірно. Підтримуюча терапія – 40 мг 1 раз на 2 тижні підшкірно.
Слід ретельно переглянути необхідність продовження терапії після 16 тижнів для пацієнтів, у яких протягом вказаного терміну не спостерігається відповіді на лікування.
Для пацієнтів, у яких не спостерігається адекватної відповіді на Хайрімоз в дозі 40 мг 1 раз на 2 тижні протягом 16 тижнів терапії, може бути ефективним підвищення дози до 40 мг 1 раз на тиждень або 80 мг 1 раз на 2 тижні. Слід ретельно переглянути співвідношення користь/ризик продовження терапії в дозі 40 мг на тиждень або 80 мг 1 раз на 2 тижні для пацієнтів, у яких не було адекватної відповіді на лікування після підвищення дози (див. розділ «Фармакодинаміка»). Якщо була досягнута адекватна відповідь після переходу на 40 мг на тиждень або 80 мг 1 раз на 2 тижні, дозу потім можна зменшити до 40 мг 1 раз на 2 тижні.
Гнійний гідраденіт (ГГ)
Рекомендований режим дозування для дорослих пацієнтів з гнійним гідраденітом – 160 мг початково на тижні 0 (день 1), дозу можна вводити у вигляді 4 ін’єкцій в один день або по 2 ін’єкції в день протягом двох днів поспіль, потім – 80 мг через 2 тижні (день 15), дозу слід вводити у вигляді 2 ін’єкцій в один день. По закінченню двох тижнів (день 29) рекомендована доза становить 40 мг 1 раз на тиждень. Протягом терапії препаратом Хайрімоз можна продовжувати приймати антибіотики, якщо це необхідно. Також рекомендовано продовжувати щоденне місцеве промивання антисептиками уражених ділянок.
Слід ретельно переглянути необхідність продовження терапії понад 12 тижнів для пацієнтів, у яких у межах цього терміну не спостерігається клінічної відповіді.
При перериванні терапії можливе повернення до застосування адалімумабу в дозі 40 мг 1 раз на тиждень або 80 мг 1 раз на 2 тижні (див. розділ «Фармакодинаміка»).
При довготривалій терапії необхідно періодично оцінювати співвідношення користь/ризик (див. розділ «Фармакодинаміка»).
Хвороба Крона
Для індукції ремісії рекомендована початкова доза для дорослих пацієнтів становить 80 мг на тижні 0 (день 1) з подальшим зменшенням дози до 40 мг на тижні 2 (день 15) підшкірно. Якщо необхідно отримати більш швидку клінічну відповідь, можна спочатку застосовувати 160 мг на тижні 0 (день 1), доза може бути введена у вигляді 4-х ін’єкцій в один день або як дві ін’єкції по 40 мг протягом двох днів поспіль, а на тижні 2 (день 15) застосовувати дозу 80 мг підшкірно. Необхідно взяти до уваги, що у такому випадку ризик виникнення побічних реакцій підвищується.
Після індукційної терапії розпочинати підтримуюче лікування у дозі 40 мг 1 раз на 2 тижні підшкірно. Альтернативно, якщо пацієнт припинив терапію і знову з’явилися симптоми захворювання, терапію лікарським засобом Хайрімоз можна розпочати знову. Існують обмежені дані щодо повторної терапії лікарським засобом Хайрімоз після перерви більше ніж на 8 тижнів від введення останньої дози. Протягом підтримуючої терапії дозу кортикостероїдів можна зменшити, зважаючи на клінічну практику.
При зменшенні клінічної відповіді деякі пацієнти можуть потребувати збільшення частоти введення препарату до 40 мг 1 раз на тиждень підшкірно або 80 мг 1 раз на 2 тижні.
Деяким пацієнтам, у яких не досягнуто клінічної відповіді на 4-й тиждень лікування, слід продовжити підтримуючу терапію до 12-го тижня. Слід ретельно переглянути необхідність продовження терапії для пацієнтів, у яких в межах цього терміну не спостерігається клінічної відповіді.
Виразковий коліт
Рекомендована початкова доза для індукції ремісії у дорослих пацієнтів з виразковим колітом помірного або тяжкого ступеня активності становить 160 мг на тижні 0 (день 1), доза може бути введена у вигляді 4-х ін’єкцій в один день або по дві ін’єкції в день протягом двох днів поспіль, та 80 мг через 2 тижні (день 15). Після індукційної терапії рекомендована доза становить 40 мг 1 раз на 2 тижні у вигляді підшкірної ін’єкції.
Протягом підтримуючої терапії дозу кортикостероїдів можна зменшити, зважаючи на клінічну практику.
При зменшенні клінічної відповіді деякі пацієнти можуть потребувати збільшення частоти введення препарату до 40 мг 1 раз на тиждень або 80 мг 1 раз на 2 тижні.
Клінічна відповідь має бути досягнута протягом 2–8 тижнів лікування. Терапію препаратом Хайрімоз можна продовжувати тільки для тих пацієнтів, які досягли клінічної відповіді протягом перших 8-ми тижнів лікування.
Увеїт
Рекомендована початкова доза препарату Хайрімоз для дорослих пацієнтів з увеїтом становить 80 мг, починаючи з першого тижня після початкової дози необхідно перейти до підтримуючої терапії – 40 мг 1 раз на 2 тижні підшкірно.
Існують обмежені дані щодо введення лише адалімумаба як стартової терапії. Терапію препаратом Хайрімоз можна розпочати в комбінації з кортикостероїдами та/або з іншими небіологічними імуномодулюючими препаратами. Через 2 тижні після початку комбінованої терапії поступово можна перейти на монотерапію препаратом Хайрімоз відповідно до клінічного досвіду.
Рекомендовано щорічно оцінювати співвідношення користь/ризик довготривалої терапії.
Особливі групи пацієнтів
Пацієнти літнього віку
Змінювати дозу препарату не потрібно.
Пацієнти з порушенням функції печінки та/або нирок
Застосування адалімумабу таким пацієнтам не досліджувалось, тому рекомендації щодо дозування відсутні.
Діти
Ювенільний ревматоїдний (ідіопатичний) артрит (ЮРА)
Поліартикулярний ювенільний ревматоїдний (ідіопатичний) артрит
Рекомендована доза лікарського засобу Хайрімоз для дітей віком від 2 років з поліартикулярною формою ЮРА залежить від маси тіла (таблиця 1). Хайрімоз застосовують 1 раз на 2 тижні підшкірно.
Таблиця 1. Дозування препарату Хайрімоз для пацієнтів з поліартикулярною формою ЮРА
|
Маса тіла |
Доза |
|
10 кг до 30 кг |
20 мг 1 раз на 2 тижні |
|
30 кг та більше |
40 мг 1 раз на 2 тижні |
Клінічна відповідь згідно з існуючими даними зазвичай досягається протягом 12 тижнів лікування. Слід переглянути необхідність продовження терапії для пацієнтів, у яких протягом вказаного терміну не спостерігається відповіді на лікування.
Хайрімоз не застосовують за цим показанням дітям віком до 2 років.
Ентезитасоційований артрит
Рекомендована доза лікарського засобу Хайрімоз для дітей віком від 6 років залежить від маси тіла (таблиця 2). Хайрімоз застосовують 1 раз на 2 тижні підшкірно.
Таблиця 2. Дозування препарату Хайрімоз для пацієнтів з ентезитасоційованим артритом
|
Маса тіла |
Доза |
|
15 кг до 30 кг |
20 мг 1 раз на 2 тижні |
|
30 кг та більше |
40 мг 1 раз на 2 тижні |
Застосування лікарського засобу Хайрімоз дітям віком до 6 років з ентезитасоційованим артритом не вивчалось.
Бляшковий псоріаз у дітей
Рекомендована доза препарату Хайрімоз для пацієнтів віком від 4 до 17 років з бляшковим псоріазом залежить від маси тіла (таблиця 3). Хайрімоз застосовують підшкірно.
Таблиця 3. Дозування препарату Хайрімоз для дітей з бляшковим псоріазом
|
Маса тіла |
Доза |
|
15 кг до 30 кг |
Початкова доза становить 20 мг на тижні 0, потім 20 мг 1 раз на 2 тижні, починаючи з тижня 1 |
|
Від 30 кг |
Початкова доза становить 40 мг на тижні 0, потім 40 мг 1 раз на 2 тижні, починаючи з тижня 1 |
Слід ретельно переглянути необхідність продовження терапії для пацієнтів, у яких протягом 16 тижнів не спостерігається клінічної відповіді.
Якщо призначено повторну терапію препаратом Хайрімоз, необхідно дотримуватись схеми лікування, зазначеної вище.
Безпека застосування адалімумабу дітям з бляшковим псоріазом вивчалась в середньому протягом 13 місяців.
Застосування адалімумабу дітям віком до 4 років з бляшковим псоріазом не вивчалось.
Гідраденіт у дітей віком від 12 років та з масою тіла не менше 30 кг Немає клінічних досліджень щодо застосування адалімумаба дітям від 12 років з гідраденітом. Дозування адалімумабу таким пацієнтам було визначено методом фармакокінетичного моделювання та симуляції (див. розділ «Фармакокінетика»).
Рекомендована доза адалімумабу становить 80 мг початково на тижні 0, потім 40 мг 1 раз на 2 тижні, починаючи з тижня 1, підшкірно.
Для пацієнтів з недостатньою відповіддю на застосування адалімумабу у дозуванні 40 мг 1 раз на 2 тижні може бути доцільним підвищення частоти застосування дози 40 мг до 1 разу на тиждень. Протягом терапії препаратом Хайрімоз можна продовжувати приймати антибіотики, якщо це необхідно. Також рекомендовано продовжувати щоденне місцеве промивання антисептиками уражених ділянок.
Слід ретельно переглянути необхідність продовження терапії понад 12 тижнів для пацієнтів, у яких у межах цього терміну не спостерігається клінічної відповіді.
При перериванні терапії можливе повернення до застосування Хайрімоз, якщо це необхідно.
При довготривалій терапії необхідно періодично оцінювати співвідношення користь/ризик (див. дані для дорослих у розділі «Фармакодинаміка»).
Адалімумаб не застосовують за цим показанням дітям віком до 12 років.
Хвороба Крона у дітей
Рекомендована доза препарату Хайрімоз для пацієнтів віком від 6 до 17 років з хворобою Крона залежить від маси тіла (таблиця 4).
Хайрімоз застосовують підшкірно.
Таблиця 4. Дозування препарату Хайрімоз для дітей із хворобою Крона
|
Маса тіла |
Індукційна доза |
Підтримуюча терапія, починаючи з тижня 4 |
|
< 40 кг |
40 мг на тижні 0 та 20 мг на тижні 2 Якщо існує потреба в більш швидкій відповіді на терапію, можна використовувати таку схему: 80 мг на тижні 0 та 40 мг на тижні 2. Але слід враховувати, що ризик побічних явищ при застосуванні більш високої індукційної дози зростає. |
20 мг 1 раз на 2 тижні |
|
≥ 40 кг |
80 мг на тижні 0 та 40 мг на тижні 2 Якщо існує потреба в більш швидкій відповіді на терапію, можна використовувати таку схему: 160 мг на тижні 0 та 80 мг на тижні 2. Але слід враховувати, що ризик побічних явищ при застосуванні більш високої індукційної дози зростає. |
40 мг 1 раз на 2 тижні |
Для пацієнтів з недостатньою відповіддю може бути доцільним збільшення частоти застосувань препарату Хайрімоз:
пацієнтам з масою тіла < 40 кг: 20 мг 1 раз на тиждень;
пацієнтам з масою тіла ≥ 40 кг: 40 мг 1 раз на тиждень або 80 мг 1 раз на 2 тижні.
Слід ретельно переглянути необхідність продовження терапії для пацієнтів, у яких протягом 12 тижнів не спостерігається клінічної відповіді.
Хайрімоз не застосовують за цим показанням дітям віком до 6 років.
Виразковий коліт (ВК) у дітей
Рекомендована доза препарату Хайрімоз для пацієнтів віком від 6 до 17 років з виразковим колітом базується на масі тіла (табл. 5). Хайрімоз вводять шляхом підшкірної ін’єкції.
Таблиця 5. Дозування препарату Хайрімоз для дітей з виразковим колітом (ВК)
|
Маса тіла |
Доза |
Підтримуюча терапія, починаючи з тижня 4* |
|
< 40 кг |
80 мг на 0-му тижні (у вигляді двох ін’єкцій по 40 мг в один день) 40 мг на 2-му тижні (вводиться як одна ін’єкція 40 мг) |
40 мг через тиждень |
|
≥ 40 кг |
160 мг на тижні 0 (у вигляді чотирьох ін’єкцій по 40 мг в один день або дві ін’єкції по 40 мг на добу два дні поспіль) 80 мг на 2-му тижні (у вигляді двох ін’єкцій по 40 мг в один день) |
80 мг кожні два тижні (у вигляді двох ін’єкцій по 40 мг в один день) |
* Пацієнти, яким виповнюється 18 років під час лікування препаратом Хайрімоз, повинні продовжувати лікування підтримуючою терапією.
Слід ретельно переглянути необхідність продовження терапії для пацієнтів, у яких протягом 8 тижнів не спостерігається клінічної відповіді.
Застосування лікарського засобу Хайрімоз дітям віком до 6 років з виразковим колітом не вивчалось.
Лікарський засіб Хайрімоз доступний в інших дозуваннях залежно від індивідуальних потреб в лікуванні.
Увеїт у дітей
Рекомендована доза лікарського засобу Хайрімоз для дітей віком від 2 років з хронічним неінфекційним увеїтом залежить від маси тіла (таблиця 6). Хайрімоз застосовують підшкірно.
Немає даних щодо застосування адалімумабу без супутньої терапії метотрексатом дітям з увеїтом.
Таблиця 6. Дозування лікарського засобу Хайрімоз дітям з увеїтом
|
Маса тіла |
Доза |
|
до 30 кг |
20 мг 1 раз на 2 тижні в комбінації з метотрексатом |
|
30 кг і більше |
40 мг 1 раз на 2 тижні в комбінації з метотрексатом |
Початкова навантажувальна доза адалімумабу становить 40 мг для пацієнтів з масою тіла до 30 кг і 80 мг для пацієнтів, маса тіла яких 30 кг і більше; її можна ввести за тиждень до початку підтримуючої терапії. Немає клінічних даних щодо введення початкової навантажувальної дози адалімумабу дітям віком до 6 років (див. розділ «Фармакокінетика»).
Застосовування Хайрімоз дітям віком до 2 років за даним показанням не обґрунтоване. Рекомендується щорічно оцінювати користь та ризик довготривалого лікування (див. розділ «Фармакодинаміка»).
Псоріатичний артрит та аксіальний спондилоартрит, включаючи анкілозуючий спондиліт
Застосування адалімумабу дітям за показаннями анкілозуючий спондиліт та псоріатичний артрит не є релевантним.
Спосіб застосування
Хайрімоз застосовують підшкірно.
Введення
Щоб уникнути можливого інфікування й забезпечити правильне використання лікарського засобу, неухильно дотримуйтеся цих інструкцій.
Перед введенням препарату Хайрімоз обов’язково прочитайте ці інструкції із застосування лікарського засобу, переконайтеся, що вам усе зрозуміло, та дотримуйтеся їх. Переш ніж ви почнете використовувати препарат Хайрімоз, ваш лікар покаже, як підготуватися та зробити ін’єкцію попередньо наповненим шприцом із однією дозою. З усіма запитаннями звертайтеся до свого лікаря.
Попередньо наповнений шприц з однією дозою лікарського засобу Хайрімоз із захисним пристроєм голки й додатковим упором для пальців
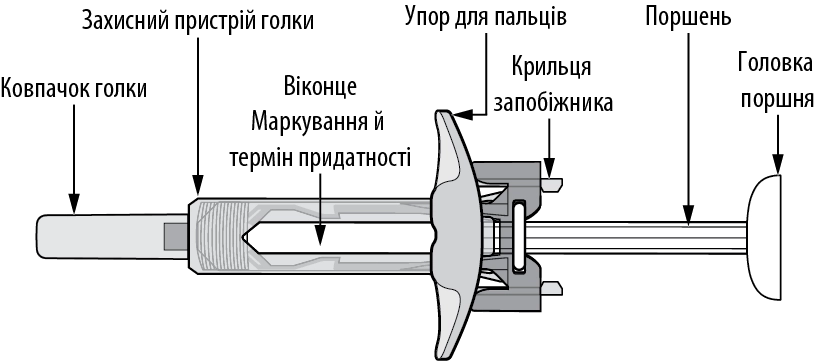
|
||
|
Рис. A. Попередньо наповнений шприц із препаратом Хайрімоз із захисним пристроєм голки й упором для пальців |
||
Обов’язково дотримуйтесь таких інструкцій:
· Не використовуйте попередньо наповнений шприц, якщо пломби блістера порушені, оскільки це може бути небезпечно.
· Не відкривайте зовнішню упаковку, доки не будете готові до використання шприца.
· Ніколи не залишайте попередньо наповнений шприц без нагляду там, де інші особи можуть мати до нього доступ.
· Якщо ви впустили шприц, не використовуйте його в разі пошкодження або від’єднання ковпачка.
· Не знімайте ковпачок, доки не будете готові до ін’єкції.
· Не торкайтесь крилець запобіжника до використання. В іншому випадку запобіжник може активуватись передчасно.
· Не знімайте упор для пальців до ін’єкції.
· Вводьте Хайрімоз через 15–30 хвилин після виймання з холодильника для більш комфортного введення.
· Негайно викиньте шприц після використання. Не використовуйте шприц повторно. Див. п. 4. «Утилізація використаних шприців» наприкінці цієї інструкції із застосування.
Умови зберігання попередньо наповненого шприца з однією дозою препарату Хайрімоз
· Зберігати в холодильнику при температурі 2–8 °С у зовнішній упаковці.
· За потреби (наприклад, на час подорожі) попередньо наповнений шприц можна зберігати за кімнатної температури (до 25 °С) не довше 42 днів, обов’язково захищаючи від світла. Після того, як шприц був вийнятий із холодильника й нагрівся до кімнатної температури, його слід використати протягом 42 днів або викинути, навіть якщо через деякий час ви знов поклали його в холодильник. Запишіть дату, коли шприц був вперше вийнятий із холодильника, і дату, після якої його потрібно викинути.
· Зберігайте попередньо наповнені шприци в оригінальній упаковці для захисту від світла.
· Не зберігайте попередньо наповнені шприци за критично високих або критично низьких температур.
· Не заморожуйте попередньо наповнені шприци.
Зберігайте препарат Хайрімоз і всі лікарські засоби в недоступному для дітей місці.
Що потрібно для ін’єкції?
Розкладіть зазначені нижче предмети на чистій рівній поверхні.
Вміст упаковки з попередньо наповненим шприцом:
· Попередньо наповнений шприц із препаратом Хайрімоз (див. рис. А). Кожен попередньо наповнений шприц містить 40 мг / 0,4 мл адалімумабу.
· Не входить до складу упаковки з попередньо наповненим шприцом із препаратом Хайрімоз (див. рис. В):
· Спиртова серветка
· Ватна кулька або бинт
· Контейнер для гострих предметів; див. п. 4 «Утилізація використаних шприців»
· Пластир

Рис. В. Предмети, що не входять до складу упаковки
|
Перед ін’єкцією |
|
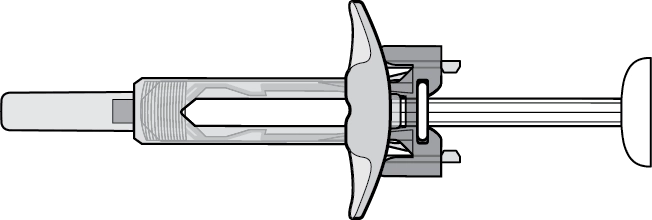
Рис. C. Запобіжник не активований – шприц готовий до використання o У цій конфігурації запобіжник НЕ АКТИВОВАНИЙ. o Шприц готовий до використання (див. рис. C). |
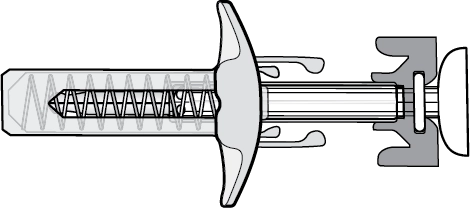
Рис. D. Запобіжник активований – не використовувати! o У цій конфігурації запобіжник АКТИВОВАНИЙ. o НЕ ВИКОРИСТОВУЙТЕ шприц (див. рис. D). |
Підготовка шприца
· Для більш комфортної ін’єкції дістаньте з холодильника попередньо наповнений шприц і залиште його невідкритим на робочій поверхні приблизно на 15–30 хвилин до досягнення кімнатної температури.
· Дістаньте попередньо наповнений шприц із блістера.
· Подивіться у віконце. Розчин повинен бути безбарвним або злегка жовтуватим, а також прозорим або злегка опалесцентним. Не використовуйте препарат, якщо в ньому спостерігаються частинки та/або наявна зміна кольору. Якщо вас турбує зовнішній вигляд розчину, зверніться за допомогою до провізора.
· Не використовуйте попередньо наповнений шприц, якщо він пошкоджений або запобіжник активований. Поверніть шприц та зовнішню упаковку до аптеки.
· Перевірте термін придатності на попередньо наповненому шприці. Не використовуйте попередньо наповнений шприц, якщо термін придатності закінчився.
Зверніться до провізора, якщо попередньо наповнений шприц не відповідає будь-якій із цих умов.
|
1. Вибір місця ін’єкції |
||||
|
· Рекомендованим місцем ін’єкції є передня частина стегон. Також препарат можна вводити у нижню частину живота, але в радіусі не менше ніж 5 см навколо пупка (див. рис. E). · Щоразу обирайте інше місце ін’єкції. · Не вводьте препарат у зони, де шкіра є чутливою, має синці, почервоніння, лущення або ущільнення. Уникайте ділянок зі шрамами або розтяжками. Якщо у вас псоріаз, НЕ ВВОДЬТЕ препарат безпосередньо в зони з бляшками. |

Рис. E. Вибір місця ін’єкції |
|||
|
2. Очищення місця ін’єкції |
||||
|
· Добре вимийте руки водою з милом. · Круговими рухами протріть місце ін’єкції спиртовим тампоном. Дайте висохнути (див. рис. F). · Не торкайтесь очищеної ділянки перед ін’єкцією. |

Рис. F. Очищення місця ін’єкції |
|||
|
3. Процедура ін’єкції |
||||
|
· Обережно змініть ковпачок зі шприца (див. рис. G). · Викиньте ковпачок. · Ви можете побачити краплю рідини на кінці голки. Це нормально. |
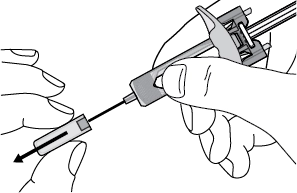
Рис. G. Зняття ковпачка |
|||
|
· Обережно прищипніть шкіру в місці ін’єкції (див. рис. H). · Введіть голку, як показано на зображенні. · Введіть голку до кінця, щоб забезпечити повне введення препарату. · Використайте шприц протягом 5 хвилин після того, як знімете ковпачок. |
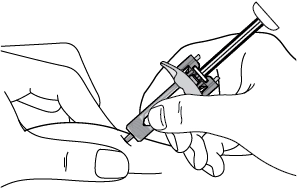
Рис. H. Введення голки |
|||
|
· Тримайте шприц, як показано на зображенні (див. рис. I). · Поступово натискайте на поршень до кінця руху, так щоб голівка поршня повністю опинилась між крильцями запобіжника. · Тримайте поршень натиснутим, утримуючи шприц на місці протягом 5 секунд. |

Рис. I. Утримування шприца |
|||
|
· Тримайте поршень повністю натиснутим, обережно виймаючи голку з місця ін’єкції та відпускаючи шкіру (див. рис. J). |
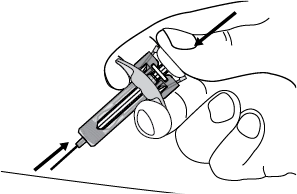
Рис. J. Виймання голки |
|||
|
· Обережно відпустіть поршень та зачекайте, доки запобіжник автоматично не закриє голку (див. рис. K). · У місці ін’єкції може проступити кров. Накрийте місце ін’єкції ватною кулькою або бинтом та тримайте протягом 10 секунд. Не тріть місце ін’єкції. У разі необхідності його можна заклеїти пластиром. - |

Рис. K. Вивільнення поршня |
|||
|
4. Утилізація використаних шприців |
||||
|
· Викиньте використаний шприц у контейнер для гострих предметів (контейнер зі стійкого до проколів матеріалу з кришкою, див. рис. L). Для власної безпеки та захисту оточуючих ніколи не використовуйте шприци й голки повторно. · Ніколи не викидайте лікарські засоби в каналізацію або разом із побутовими відходами. Запитайте лікаря або провізора, як правильно позбутися ліків, які вам більше не потрібні. Ці заходи допоможуть захистити довкілля. Усі невикористані засоби або відходи слід утилізувати з дотриманням вимог місцевого законодавства. |
 Рис. L. Утилізація
використаного попередньо наповненого шприца
Рис. L. Утилізація
використаного попередньо наповненого шприца
|
|||
Якщо у вас виникли запитання, зверніться до свого лікаря, провізора або медсестри, які знайомі з особливостями використання препарату Хайрімоз.
Попередньо наповнений шприц може зберігатися при температурі максимум до 25 °C протягом періоду до 42 днів. Попередньо наповнений шприц слід зберігати у захищеному від світла місці та утилізувати, якщо він не використовується протягом 42-денного періоду.
Діти
Показаний для застосування дітям згідно з розділом «Показання».
Передозування
У ході клінічних досліджень адалімумабу не було виявлено випадків дозолімітуючої токсичності. Пацієнтам призначалися багаторазові дози до 10 мг/кг, що приблизно в 15 разів більше рекомендованої дози. Таке застосування не супроводжувалось ознаками токсичності, пов’язаної із передозуванням.
Побічні реакції
Загальна інформація щодо профілю безпеки
Адалімумаб досліджували у контрольованих клінічних дослідженнях та дослідженнях відкритого періоду тривалістю близько 60 місяців чи більше за участю 9506 пацієнтів. Ці дослідження включали пацієнтів з раннім та довготривалим ревматоїдним артритом, ЮРА (поліартикулярним ювенільним ідіопатичним артритом та ентезитасоційованим артритом), а також із аксіальним спондилоартритом (анкілозуючий спондиліт та нерентгенографічний аксіальний спондилоартрит), псоріатичним артритом, хворобою Крона, виразковим колітом, псоріазом, гнійним гідраденітом, увеїтом. Нижче приведено дані, отримані під час основних контрольованих досліджень, в яких 6089 пацієнтам застосовували адалімумаб та 3801 пацієнту застосовували плацебо або препарат порівняння впродовж контрольованого періоду.
Протягом основних клінічних випробувань 5,9 % пацієнтів, які отримували адалімумаб, та 5,4 % пацієнтів з контрольної групи припинили лікування через побічні реакції.
Найчастіше повідомлялось про виникнення побічних реакцій у вигляді інфекцій (таких як назофарингіт, інфекції верхніх відділів дихальних шляхів та синусит), реакцій в місці введення (почервоніння, свербіж, геморагії, біль або набряк), головний біль та скелетно-м’язовий біль.
Повідомлялося про серйозні побічні реакції при застосуванні адалімумабу. Антагоністи ФНП, такі як Хайрімоз, впливають на імунну систему, їх застосування може спричинити зниження опірності організму до інфекцій та злоякісних новоутворень.
Під час застосування адалімумабу повідомлялося про виникнення інфекцій, які можуть становити загрозу життю людини та призвести до смерті (включаючи сепсис, опортуністичні інфекції та туберкульоз), про реактивацію гепатиту В та виникнення різних новоутворень (включаючи лейкемію, лімфому та гепатолієнальну Т-клітинну лімфому).
Повідомлялось також про серйозні гематологічні, неврологічні та аутоімунні реакції. Ці реакції включали поодинокі випадки панцитопенії, апластичної анемії, випадки центральних та периферичних демієлінізуючих розладів, виникнення вовчака, вовчакоподібних станів та синдрому Стівенса – Джонсона.
Діти
Зазвичай побічні реакції, що виникали у дітей, були однакові за частотою та характером з побічними реакціями, які спостерігалися у дорослих пацієнтів.
У таблиці 7 представлено побічні реакції з можливим причинно-наслідковим зв’язком, які спостерігалися протягом клінічних випробувань та у постмаркетинговий період. Побічні реакції зазначено за органами і системами організму та частотою виникнення (≥ 1/10 – дуже часті, від ≥1/100 до ˂1/10 – часті; від ≥ 1/1000 до ˂1/100 – нечасті, від ≥1/10000 до ˂1/1000 – поодинокі; частота невідома (не може бути оцінена за наявними даними)). У межах кожної групи за частотою виникнення побічні реакції наведені в порядку зменшення їхньої серйозності.
Найвища частота виникнення побічних реакцій, зафіксована серед різних показань, була включена у таблицю нижче. Зірочка (*) у стовпці «Органи і системи організму» вказує на наявність додаткової інформації в розділах «Протипоказання», «Особливості застосування» та «Побічні реакції».
Таблиця 7
|
Органи і системи організму |
Частота |
Побічні реакції |
|
Інфекції та інвазії* |
дуже часті |
інфекції дихальних шляхів (включаючи інфекції нижніх та верхніх відділів дихальних шляхів, пневмонію, синусит, фарингіт, ринофарингіт, пневмонію, спричинену вірусом герпесу); |
|
часті |
системні інфекції (включаючи сепсис, кандидоз та грип), кишкові інфекції (включаючи вірусний гастроентерит), інфекції шкіри та м’яких тканин (пароніхія, целюліт, імпетиго, некротичний фасциїт, оперізуючий герпес), інфекції вуха, інфекції ротової порожнини (включаючи вірус простого герпесу, герпес ротової порожнини та інфекції зубів), інфекції статевих органів (включаючи грибковий вульвовагініт), інфекції сечовивідних шляхів (включаючи пієлонефрит), грибкові інфекції, інфекції суглобів; |
|
|
нечасті |
неврологічні інфекції (включаючи вірусний менінгіт), опортуністичні інфекції та туберкульоз (включаючи кокцидіоїдомікоз, гістоплазмоз та інфекції комплексу mycobacterium avium), бактеріальні інфекції, інфекції ока, , дивертикуліт1 |
|
|
Доброякісні, злоякісні та неспецифічні новоутворення (включаючи кісти та поліпи)* |
часті |
рак шкіри, за винятком меланоми (включаючи базальноклітинну карциному та плоскоклітинну карциному); доброякісні новоутворення; |
|
нечасті |
лімфома**, новоутворення паренхіматозних органів (включаючи рак молочної залози, пухлину легенів та пухлину щитовидної залози), меланома**; |
|
|
поодинокі |
лейкоз1; |
|
|
частота невідома |
гепатолієнальна Т-клітинна лімфома1, карцинома Меркеля (нейроендокринна карцинома шкіри)1 , саркома Капоші |
|
|
Порушення з боку кровоносної та лімфатичної систем* |
дуже часті |
лейкопенія (включаючи нейтропенію та агранулоцитоз), анемія; |
|
часті |
лейкоцитоз, тромбоцитопенія; |
|
|
нечасті |
ідіопатична тромбоцитопенічна пурпура; |
|
|
поодинокі |
панцитопенія |
|
|
Порушення з боку імунної системи* |
часті |
гіперчутливість, алергія (включаючи сезонну алергію); |
|
нечасті |
саркоїдоз1, васкуліт; |
|
|
поодинокі |
анафілаксія1 |
|
|
Порушення обміну речовин, метаболізму |
дуже часті |
підвищення рівня ліпідів крові; |
|
часті |
гіпокаліємія, гіперурикемія, відхилення від норми концентрації натрію у плазмі крові, гіпокальціємія, гіперглікемія, гіпофосфатемія, дегідратація |
|
|
Психічні розлади |
часті |
зміни настрою (включаючи депресію), тривога, безсоння |
|
Неврологічні розлади* |
дуже часті |
головний біль; |
|
часті |
парестезія (включаючи гіпестезію), мігрень, стиснення нервових корінців; |
|
|
нечасті |
інсульт1, тремор, невропатія; |
|
|
поодинокі |
розсіяний склероз, демієлінізуючі розлади (наприклад, неврит зорового нерва, синдром Гійєна – Барре)1 |
|
|
Порушення з боку органів зору |
часті |
порушення гостроти зору, кон’юнктивіт, блефарит, набряк ока; |
|
нечасті |
диплопія |
|
|
Порушення з боку органів слуху та вестибулярного апарату |
часті нечасті |
вертиго; глухота, дзвін у вухах |
|
Кардіальні порушення* |
часті |
тахікардія; |
|
нечасті |
інфаркт міокарда1, аритмія, хронічна серцева недостатність; |
|
|
поодинокі |
зупинка серця |
|
|
Судинні розлади |
часті |
артеріальна гіпертензія, припливи, гематома; |
|
нечасті |
аневризма аорти, оклюзія артерій, тромбофлебіт |
|
|
Порушення з боку дихальної системи, органів грудної клітки та середостіння* |
часті |
астма, диспное, кашель; |
|
нечасті |
легенева емболія1, хронічне обструктивне захворювання легенів, інтерстиціальне захворювання легенів, пневмоніт, плевральний випіт1; |
|
|
поодинокі |
легеневий фіброз1 |
|
|
Шлунково-кишкові розлади |
дуже часті |
біль у животі, нудота та блювання; |
|
часті |
шлунково-кишкова кровотеча, диспепсія, гастроезофагеальний рефлюкс, сухий синдром (синдром Шегрена); |
|
|
нечасті |
панкреатит, дисфагія, набряк обличчя; |
|
|
поодинокі |
перфорація кишечника1 |
|
|
Розлади гепатобіліарної системи* |
дуже часті |
підвищення рівня печінкових ферментів; |
|
нечасті |
холецистит та холелітіаз, підвищення рівня білірубіну, стеатоз печінки; |
|
|
поодинокі |
гепатит, реактивація гепатиту В1, аутоімунний гепатит1; |
|
|
частота невідома |
печінкова недостатність1 |
|
|
Зміни з боку шкіри і підшкірної клітковини |
дуже часті |
висип (включаючи ексфоліативний висип); |
|
часті |
нові випадки або погіршення перебігу псоріазу (у тому числі долонно-підошовного пустульозного псоріазу)1, свербіж, кропив’янка, екхімози (включаючи пурпуру), дерматит (включаючи екзему), оніхоклазія, підвищена пітливість, алопеція1; |
|
|
нечасті |
нічна пітливість, рубці; |
|
|
поодинокі |
мультиформна еритема1, синдром Стівенса – Джонсона1, ангіоневротичний набряк1, шкірний васкуліт1, ліхеноїдна реакція шкіри1; |
|
|
частота невідома |
погіршення симптомів дерматоміозиту1 |
|
|
Порушення з боку опорно-рухової системи та сполучної тканини |
дуже часті |
скелетно-м’язовий біль; |
|
часті |
спазми м’язів (включаючи підвищення рівня креатинфосфокінази у плазмі крові); |
|
|
нечасті |
рабдоміоліз, системний червоний вовчак; |
|
|
поодинокі |
вовчакоподібний синдром1 |
|
|
Розлади з боку сечовидільної системи |
часті |
гематурія, ниркова недостатність; |
|
нечасті |
ніктурія |
|
|
Розлади з боку репродуктивної системи та молочних залоз |
нечасті |
еректильна дисфункція |
|
Загальні розлади та реакції у місці введення* |
дуже часті |
реакції у місці введення (включаючи почервоніння у місці введення); |
|
часті |
біль у грудях, набряк, пірексія1; |
|
|
нечасті |
запалення |
|
|
Лабораторні дослідження* |
часті частота невідома |
коагуляція та порушення системи згортання крові (включаючи подовження активованого частково тромбопластинового часу (АЧТЧ)), позитивні тести на аутоантитіла (включаючи антитіла до дволанцюгової ДНК), підвищення рівня лактатдегідрогенази у плазмі крові; збільшення маси тіла2 |
|
Пошкодження, отруєння та процедурні ускладнення* |
часті |
повільне загоювання |
* Див. також розділи «Протипоказання», «Особливості застосування», «Побічні реакції».
** Включаючи відкритий період досліджень.
1 Включаючи дані спонтанних повідомлень.
2 Середня зміна маси тіла від вихідного рівня коливалася від 0,3 кг до 1,0 кг при застосуванні адалімумабу за показаннями для дорослих порівняно з (мінус) -0,4 кг до 0,4 кг при застосуванні плацебо протягом періоду лікування 4–6 місяців. Збільшення маси тіла на 5–6 кг також спостерігався у довгостроковому розширеному дослідженні із середньою експозицією приблизно 1–2 роки без контрольної групи, особливо в пацієнтів із хворобою Крона та виразковим колітом. Механізм цього ефекту незрозумілий, але може бути пов’язаний з протизапальною дією адалімумабу.
Гнійний гідраденіт
Профіль безпеки для пацієнтів із ГГ, що отримували лікування адалімумабом щотижня, відповідає відомому профіль безпеки адалімумабу.
Увеїт
Профіль безпеки для пацієнтів з увеїтом, які отримували адалімумаб 1 раз на 2 тижні, відповідає відомому профілю безпеки адалімумабу.
Опис окремих побічних реакцій
Реакції у місці введення
У контрольованих клінічних дослідженнях у дорослих та дітей, які отримували адалімумаб, у 12,9 % випадків розвинулися реакції у місці введення (еритема та/або свербіж, крововилив, біль або набряк), порівняно з 7,2 % пацієнтів контрольної групи. Більшість реакцій були легкими та загалом не потребували відміни препарату.
Інфекції
У контрольованих клінічних дослідженнях у дорослих та дітей рівень інфекцій становив 1,51/пацієнто-рік у групі пацієнтів, які отримували адалімумаб, та 1,46/пацієнто-рік у контрольній групі пацієнтів. Рівень серйозних інфекцій становив 0,04/пацієнто-рік у групі пацієнтів, які отримували адалімумаб, та 0,03/пацієнто-рік у контрольній групі пацієнтів. Переважно це були назофарингіт, інфекції верхніх дихальних шляхів та синусит. Більшість пацієнтів продовжили застосовувати адалімумаб після одужання.
У контрольованих та відкритих дослідженнях у дорослих та дітей повідомлялося про розвиток тяжких інфекцій (з летальним наслідком у поодиноких випадках): туберкульозу (у тому числі міліарного та позалегеневої локалізації) та інвазивних опортуністичних інфекцій (таких як дисемінований гістоплазмоз, пневмоцистна пневмонія, аспергільоз, лістеріоз). Більшість випадків захворювання на туберкульоз зафіксовано протягом перших восьми місяців після початку терапії і може відображати рецидив прихованої хвороби.
Новоутворення та лімфопроліферативні розлади
Протягом клінічних досліджень адалімумабу у дітей з ЮРА (поліартикулярним артритом та ентезитасоційованим артритом) злоякісні новоутворення не спостерігалися (n = 249, 655,6 пацієнто-року).
Додатково не спостерігалося злоякісних новоутворень у клінічних дослідженнях у дітей з хворобою Крона (n = 192; 498,1 пацієнто-року), бляшковим псоріазом (n = 77; 80,0 пацієнто-року), увеїтом (n = 60; 58,4 пацієнто-року).
Під час контрольованих періодів основних досліджень застосування адалімумабу дорослим протягом щонайменше 12 тижнів у пацієнтів з ревматоїдним артритом від середнього до високого ступеня активності, пацієнтів із псоріатичним артритом, аксіальним спондилоартритом (анкілозуючим спондилітом та нерентгенографічним аксіальним спондилоартритом), хворобою Крона, виразковим колітом, гнійним гідраденітом, увеїтом та псоріазом рівень новоутворень (за винятком лімфоми та немеланомного раку шкіри) становив (95 % довірчий інтервал) 6,8 (4,4; 10,5) на 1000 пацієнто-років у 5291 пацієнта, які приймали адалімумаб, в порівнянні з рівнем 6,3 (3,4; 11,8) на 1000 пацієнто-років у 3444 пацієнтів контрольної групи (середня тривалість лікування становила 4,0 місяця у групі застосування адалімумабу та 3,8 місяця у пацієнтів контрольної групи). Рівень немеланомного раку шкіри (95 % довірчий інтервал) становив 8,8 (6,0; 13,0) на 1000 пацієнто-років у пацієнтів, які приймали адалімумаб, та 3,2 (1,3; 7,6) на 1000 пацієнто-років у пацієнтів контрольної групи. Серед наведених випадків частота виникнення раку шкіри, плоскоклітинної карциноми (95 % довірчий інтервал) становила 2,7 (1,4; 5,4) на 1000 пацієнто-років у пацієнтів, які приймали адалімумаб, та 0,6 (0,1; 4,5) на 1000 пацієнто-років у пацієнтів контрольної групи. Рівень лімфом (95 % довірчий інтервал) становив 0,7 (0,2; 2,7) на 1000 пацієнто-років у пацієнтів, які приймали адалімумаб, та 0,6 (0,1; 4,5) на 1000 пацієнто-років у пацієнтів контрольної групи.
Темпи розвитку новоутворень, що спостерігалися (за винятком лімфоми та немеланомного раку шкіри), становлять приблизно 8,5/1000 пацієнто-років у контрольованих дослідженнях та у дослідженнях відкритого періоду, які ще тривають та вже завершені. Темпи розвитку немеланомного раку шкіри становили приблизно 9,6/1000 пацієнто-років, а темпи розвитку лімфом – приблизно 1,3/1000 пацієнто-років. Ці дослідження тривали приблизно 3,3 року та включали 6427 пацієнтів, які отримували адалімумаб принаймні протягом 1 року або в яких новоутворення виникли упродовж року від початку терапії, що становить більш ніж 26439 пацієнто-років терапії.
У постмаркетинговий період із січня 2003 року по грудень 2010 року переважно у пацієнтів з ревматоїдним артритом, які лікувалися адалімумабом, рівень злоякісних новоутворень становив приблизно 2,7 на 1000 пацієнто-років. Зафіксовано рівні немеланомного раку шкіри та лімфом приблизно 0,2 та 0,3 на 1000 пацієнто-років відповідно (див. розділ «Особливості застосування»).
У постмаркетинговій практиці у поодиноких випадках у пацієнтів, які застосовували адалімумаб, повідомлялося про розвиток гепатолієнальної Т-клітинної лімфоми (див. розділ «Особливості застосування»).
Аутоантитіла
У ході клінічних досліджень ревматоїдного артриту 1–5 фази пацієнтам декілька разів проводили аналіз крові на наявність аутоантитіл. У цих контрольованих дослідженнях у 11,9 % пацієнтів, які приймали адалімумаб, та у 8,1 % пацієнтів групи плацебо повідомлялося про позитивні титри, при активному моніторингу лікування спостерігалися негативні титри антинуклеарних антитіл на 24 тижні. У двох пацієнтів (із 3441 пацієнтів з РА, ПсА та АС, які отримували адалімумаб протягом клінічних випробувань) розвинулися ознаки вовчакоподібного синдрому (вперше виявленого), що зникли після припинення лікування. У жодного пацієнта не розвинулися люпус-нефрит або ураження центральної нервової системи.
Активність печінкових ферментів
У контрольованих клінічних дослідженнях 3 фази за участю пацієнтів з ревматоїдним артритом та псоріатичним артритом протягом контрольованого періоду тривалістю від 4 до 104 тижнів підвищення АЛТ (аланінтрансаміназа) у 3 або більше разів від верхньої межі норми спостерігалося у 3,7 % пацієнтів, які отримували адалімумаб, та у 1,6 % пацієнтів контрольної групи.
У контрольованих клінічних дослідженнях 3 фази за участю пацієнтів віком 4–17 років з поліартикулярним артритом та пацієнтів віком 6–17 років з ентезитасоційованим артритом підвищення АЛТ у 3 або більше разів від верхньої межі норми спостерігалося у 6,1 % пацієнтів, які отримували адалімумаб, і 1,3 % пацієнтів контрольної групи. Більшість випадків підвищення АЛТ спостерігалося під час супутньої терапії метотрексатом. Не спостерігалось підвищення АЛТ у 3 або більше разів від верхньої межі норми у клінічних дослідженнях 3 фази у пацієнтів з поліартикулярним артритом віком 2–4 роки.
У контрольованих клінічних дослідженнях 3 фази за участю пацієнтів із хворобою Крона та виразковим колітом з тривалістю контрольованого періоду від 4 до 52 тижнів підвищення АЛТ у 3 або більше разів від верхньої межі норми спостерігалося у 0,9 % пацієнтів обох груп.
У клінічному дослідженні 3 фази за участю дітей з хворобою Крона, де було оцінено ефективність та безпеку двократного відносно маси тіла режиму дозування з подальшим приведенням до режиму дозування відповідно до маси тіла з тривалістю терапії до 52 тижнів, підвищення АЛТ в 3 або більше разів вище верхньої межі норми спостерігалось у 2,6 % (5/192) пацієнтів, 4 з яких отримували адалімумаб на тлі одночасного застосування імуносупресантів.
У контрольованих клінічних дослідженнях 3 фази за участю пацієнтів з бляшковим псоріазом з тривалістю контрольного періоду від 12 до 24 тижнів підвищення АЛТ у 3 або більше разів від верхньої межі норми спостерігалося у 1,8 % пацієнтів обох груп.
У контрольованих клінічних дослідженнях (початкова доза 160 мг (тиждень 0) і 80 мг (тиждень 2), а потім 40 мг 1 раз на тиждень починаючи з тижня 4) за участю пацієнтів з гнійним гідраденітом з тривалістю контрольованого періоду від 12 до 16 тижнів підвищення АЛТ у 3 або більше разів від верхньої межі норми спостерігалося у 0,3 % пацієнтів, які отримували адалімумаб, та у 0,6 % пацієнтів контрольної групи.
У контрольованих клінічних дослідженнях (початкова доза 80 мг (тиждень 0), а потім, починаючи з тижня 1, по 40 мг 1 раз на 2 тижні) за участю пацієнтів з увеїтом з тривалістю контрольного періоду до 80 тижнів (представлені середні значення 166,5 дня та 105 днів у групі терапії адалімумабом та контрольній групі відповідно) підвищення АЛТ у 3 або більше разів від верхньої межі норми спостерігалося у 2,4 % пацієнтів, які отримували адалімумаб, та у 2,4 % пацієнтів контрольної групи.
У контрольованому дослідженні 3 фази застосування адалімумабу дітям з виразковим колітом (N = 93), в якому оцінювали ефективність та безпеку застосування підтримуючої дози 0,6 мг/кг (максимум 40 мг) при введенні один раз на 2 тижні (N = 31) та підтримуючої дози 0,6 мг/кг (максимум 40 мг) при введенні щотижня (N = 32) після застосування індукційної дози залежно від маси тіла 2,4 мг/кг (максимум 160 мг) на тижні 0 і тижні 1 та дози 1,2 мг/кг (максимум 80 мг) на тижні 2 (N = 63) або після застосування індукційної дози 2,4 мг/кг (максимум 160 мг) на тижні 0, плацебо на тижні 1 та дози 1,2 мг/кг (максимум 80 мг) на тижні 2 (N = 30), випадки підвищення активності АЛТ у 3 або більше разів від верхньої межі норми спостерігались у 1,1 % (1/93) пацієнтів.
При застосуванні за всіма показаннями у клінічних випробуваннях пацієнти мали безсимптомне підвищення рівня АЛТ і в більшості випадків підвищення було минущим на тлі тривалого лікування. Однак були дуже рідкісні постмаркетингові повідомлення про печінкову недостатність та менш серйозні печінкові реакції, що можуть призвести до печінкової недостатності, такі як гепатит, включаючи аутоімунний гепатит, у хворих, які отримували адалімумаб.
Супутня терапія з азатіоприном/6-меркаптопурином
У дослідженнях у дорослих пацієнтів з хворобою Крона, які отримували адалімумаб у комбінації з азатіоприном/6-меркаптопурином, спостерігалося підвищення частоти виникнення новоутворень та тяжких інфекцій порівняно з пацієнтами, які отримували монотерапію адалімумабом.
Повідомлення про побічні реакції після реєстрації лікарського засобу має важливе значення. Це дає змогу проводити моніторинг співвідношення користь/ризик при застосуванні цього лікарського засобу. Медичним та фармацевтичним працівникам, а також пацієнтам або їхнім законним представникам слід повідомляти про усі випадки підозрюваних побічних реакцій та відсутності ефективності лікарського засобу через Автоматизовану інформаційну систему з фармаконагляду за посиланням: https://aisf.dec.gov.ua.
Термін придатності. 2 роки.
Не слід застосовувати препарат після закінчення терміну придатності.
Умови зберігання
Зберігати при температурі 2–8 °С в оригінальній упаковці для захисту від світла. Не заморожувати. Зберігати у недоступному для дітей місці.
Дозволяється зберігати попередньо наповнений шприц при температурі не вище 25 °C протягом не більше 42 діб. Попередньо наповнений шприц слід зберігати у захищеному від світла місці та утилізувати, якщо він не був використаний протягом 42 діб.
Несумісність
У зв’язку з тим, що дослідження сумісності цього лікарського засобу не проводилися, його не можна змішувати з іншими лікарськими засобами.
Упаковка
По 40 мг / 0,4 мл розчину в попередньо наповненому шприці; по 2 попередньо наповнених шприців у блістерах у картонній коробці.
Категорія відпуску. За рецептом.
Виробник
Новартіс Фармасьютікал Мануфактурінг ГмбХ
або
Сандоз ГмбХ – Виробнича дільниця Асептичні лікарські засоби Шафтенау (Асептичні ЛЗШ)
Місцезнаходження виробника та адреса місця провадження його діяльності
Біохеміштрассе 10, Унтерлангкампфен, Лангкампфен, 6336, Австрія
або
Біохеміштрассе 10, 6336 Лангкампфен, Австрія
