ГІМПАВЗІ
-
США Пфайзер Ейч.Сі.Пі. КорпорейшнDosage form: розчин для ін’єкцій, 150 мг/мл; 1 попередньо наповнена ручка, що містить шприц, у картонній коробці з маркуванням українською та англійською мовамиComposition: 1 попередньо наповнена ручка містить 150 мг марстацимабу в 1 мл розчинуMedicinal dispensing terms: за рецептомСertificate number: UA/21237/01/01ATS code: B02BX11Expiry: 3 роки.
ІНСТРУКЦІЯ
для медичного застосування лікарського засобу
ГIМПАВЗІ
(HYMPAVZI)
Склад:
діюча речовина: марстацимаб;
1 попередньо наповнена ручка містить 150 мг марстацимабу в 1 мл розчину;
допоміжні речовини: L-гістидин, L-гістидину моногідрохлорид, сахароза, динатрію едетат, полісорбат 80 (E433), вода для ін’єкцій.
Лікарська форма. Розчин для ін’єкцій.
Основні фізико-хімічні властивості: прозорий, від безбарвного до світло-жовтого кольору розчин з рН 5,8.
Фармакотерапевтична група
Антигеморагічні лікарські засоби. Вітамін K та інші гемостатичні лікарські засоби. Інші гемостатичні лікарські засоби для системного застосування.
Код АТХ B02B X11.
Фармакологічні властивості
Фармакодинаміка
Механізм дії
Марстацимаб є моноклональним антитілом людини IgG1, спрямованим проти домену Куніца 2 (K2) інгібітора тканинного фактора, основного інгібітора зовнішньої системи коагуляції. Інгібітор тканинного фактора спочатку зв’язується з активним центром фактора Xa та інгібує його через другий інгібіторний домен Куніца (K2). Дія марстацимабу, який нейтралізує інгібіторну активність інгібітора тканинного фактора, може сприяти посиленню зовнішньої системи та обходу дефіцитів внутрішньої системи коагуляції шляхом збільшення кількості вільного фактора Xa для збільшення вироблення тромбіну та сприяння гемостазу.
Фармакодинамічна дія
Як передбачає механізм інгібування тканинного фактора, введення марстацимабу пацієнтам з гемофілією спричиняє збільшення загального рівня інгібітора тканинного фактора і біомаркерів подальшого створення тромбіну, як-от фрагменти протромбіну 1 + 2, піковий рівень тромбіну і D-димеру. Ці зміни були оборотними після припинення терапії. Про спорадичне або тимчасове збільшення кількості D‑димеру і фрагментів протромбіну 1 + 2 до рівня, який перевищує фізіологічні значення, повідомляли в дослідженні III фази. Проблеми з безпекою не виникали.
Клінічна ефективність і безпека
Клінічні дослідження у дорослих пацієнтів і пацієнтів дитячого віку з гемофілією А без вироблення інгібіторів FVIII або гемофілією B без вироблення інгібіторів FIX
Пацієнти (віком ≥ 12 років і з масою тіла ≥ 35 кг) з гемофілією А без вироблення інгібіторів та гемофілією B без вироблення інгібіторів (дослідження B7841005)
Ключове дослідження III фази було однофакторним перехресним відкритим багатоцентровим дослідженням із залученням 116 дорослих пацієнтів і пацієнтів дитячого віку чоловічої статі (віком від 12 років і з масою тіла ≥ 35 кг) з тяжкою гемофілією A без вироблення інгібіторів FVIII або тяжкою гемофілією B без вироблення інгібіторів FIX, які раніше отримували лікування FVIII або FIX за необхідності (N = 33) або як профілактику (N = 83). Пацієнтів, які раніше або на момент дослідження лікували ішемічну хворобу серця, венозний або артеріальний тромбоз або ішемічну хворобу чи мають такі захворювання в анамнезі, виключали з дослідження.
Досліджувана популяція характеризувалася фенотипом тяжкої кровотечі. Середня річна частота кровотечі становила 38,00 і 7,85 протягом 6-місячної фази спостереження для когорт лікування за необхідності та профілактичного лікування відповідно до переходу на щотижневу профілактику марстацимабом. Усі пацієнти (100 %) в когорті лікування за необхідності мали один або кілька суглобів-цілей на початку дослідження, а 36 % мали 3 або більше суглобів-цілей на початку дослідження. У когорті планового профілактичного лікування 56,6 % пацієнтів мали один або більше суглобів-цілей на початку дослідження, а 15,7 % мали 3 або більше суглобів-цілей на початку дослідження.
Після 6-місячної фази спостереження, протягом якої проводили замісну факторну терапію за необхідності або планову профілактику, пацієнти отримали початкову навантажувальну дозу 300 мг марстацимабу, а потім підтримувальні дози 150 мг марстацимабу один раз на тиждень протягом 12 місяців. Підвищення дози до 300 мг марстацимабу один раз на тиждень було дозволено через 6 місяців для пацієнтів з масою тіла ≥ 50 кг, які зазнали 2 або більше проривних кровотеч. Чотирнадцятьом (12,1 %) зі 116 пацієнтів, які отримували марстацимаб протягом принаймні 6 місяців, підвищили підтримувальну дозу.
Середній вік пацієнтів в усіх групах лікування становив 32,4 року (мінімальний вік — 13 років, максимальний — 66 років), 16,4 % пацієнтів були віком від 12 до < 18 років, 83,6 % – віком від 18 років, 100 % – чоловічої статі. У цьому дослідженні 48,3 % пацієнтів були представниками європеоїдної раси, 50,0 % — азійського походження, 0,9 % — африканцями або афроамериканцями, а для 0,9 % інформація щодо расової приналежності відсутня; 10,3 % пацієнтів зазначили, що мають іспанське або латиноамериканське походження. У жодного з пацієнтів не вироблялися інгібітори (78,4 % – з гемофілією А, 21,6 % – з гемофілією B).
Основною метою дослідження з точки зору ефективності було порівняння профілактичного лікування марстацимабом протягом фази активного лікування з плановим профілактичним лікуванням факторами протягом фази спостереження. Показником ефективності була середня річна частота кровотеч, які потребували лікування. Інші ключові цілі дослідження з точки зору ефективності включали оцінку профілактичного лікування марстацимабом порівняно з плановим профілактичним лікуванням факторами на основі частоти спонтанних кровотеч, суглобових кровотеч, кровотеч у суглобах-цілях, а також оцінку якості життя пацієнтів, пов’язаної зі здоров’ям (HRQoL).
У таблиці 1 наведено результати оцінювання ефективності профілактичного лікування марстацимабом порівняно з плановим профілактичним лікуванням факторами. Марстацимаб продемонстрував не меншу ефективність та статистичну перевагу над плановою профілактикою факторами (вимірювали середню річну частоту кровотеч, які потребували лікування).
Таблиця 1. Порівняння середньої річної частоти кровотеч у разі проведення профілактичного лікування препаратом Гімпавзі та попереднього планового профілактичного лікування факторами зсідання в пацієнтів віком ≥ 12 років без вироблення інгібіторів фактора VIII або фактора IX
|
Кінцеві точки в порядку ієрархії випробування |
Планове профілактичне лікування факторами протягом 6‑місячної фази спостереження (N = 83) |
Профілактичне лікування препаратом Гімпавзі протягом 12‑місячної фази активного лікування (N = 83) |
|
Кровотечі, які потребували лікування (первинні) |
||
|
Середня річна частота кровотеч, на основі моделі (95 % ДІ) |
7,85 (5,09; 10,61) |
5,08 (3,40; 6,77) |
|
Різниця порівняно з плановим профілактичним лікуванням (95 % ДІ) |
–2,77 (–5,37, –0,16) p-значення = 0,0376* |
|
|
Учасники без кровотеч, n (%) |
33 (39,8) |
29 (34,9) |
|
Спонтанні кровотечі, які потребували лікування |
||
|
Середня річна частота кровотеч, на основі моделі (95 % ДІ) |
5,86 (3,54; 8,19) |
3,78 (2,25; 5,31) |
|
Різниця порівняно з плановим профілактичним лікуванням (95 % ДІ) |
-2,09 (-4,23, 0,06) Не менша ефективність* |
|
|
Суглобові кровотечі, які потребували лікування |
||
|
Середня річна частота кровотеч, на основі моделі (95 % ДІ) |
5,66 (3,33; 7,98) |
4,13 (2,59; 5,67) |
|
Різниця порівняно з плановим профілактичним лікуванням (95 % ДІ) |
-1,53 (-3,70, 0,64) Не менша ефективність* |
|
|
Загальна кількість кровотеч, які потребували і не потребували лікування |
||
|
Середня річна частота кровотеч, на основі моделі (95 % ДІ) |
8,84 (5,97; 11,72) |
5,97 (4,13; 7,81) |
|
Різниця порівняно з плановим профілактичним лікуванням (95 % ДІ) |
–2,87 (–5,61, –0,12) Не менша ефективність* |
|
|
Кровотечі в суглобах-цілях, які потребували лікування |
||
|
Середня річна частота кровотеч, на основі моделі (95 % ДІ) |
3,36 (1,59; 5,14) |
2,51 (1,25; 3,76) |
|
Різниця порівняно з плановим профілактичним лікуванням (95 % ДІ) |
-0,86 (-2,41, 0,70) Не менша ефективність* |
|
* Критерій дотримано (не менша ефективність або p-значення, якщо досягнуто переваги).
· Зазначений у протоколі критерій не меншої ефективності (вище 95 % ДІ для різниці) становив 2,5 для кровотеч, які потребували лікування, спонтанних кровотеч, суглобових кровотеч; 1,2 для кровотеч у суглобах-цілях; 2,9 для загальної кількості кровотеч. Якщо критерій не меншої ефективності був дотриманий, надалі перевіряли наявність переваги та встановлювали, чи довірчий інтервал виключав нуль.
· p-значення використовували для визначення переваги.
· Розрахункові середні значення, різниця та довірчі інтервали (ДІ) для середньої річної частоти кровотеч розраховані на базі моделі негативної біноміальної регресії.
· Визначення кровотечі адаптовані на основі критеріїв Міжнародного товариства з тромбозу та гемостазу (ISTH).
· Кровотечі, які потребували лікування, — кровотечі, які лікували за допомогою FVIII або FIX.
· Загальна кількість кровотеч, — кровотечі, які лікували і не лікували за допомогою FVIII або FIX.
· ДІ — довірчий інтервал.
Проміжний аналіз дослідження B7841007
У відкритому продовженні ключового дослідження III фази 87 пацієнтів отримували марстацимаб у дозах, встановлених під час участі в дослідженні B7841005 (тобто 150 мг або 300 мг підшкірно один раз на тиждень), протягом додаткового періоду до 16 місяців (середній період 7 місяців). Дослідження продемонструвало, що марстацимаб зберігає довгострокову (> 12 місяців) ефективність без появи нових сигналів небезпеки.
Був виконаний описовий аналіз для оцінки ефективності профілактичного лікування марстацимабом із плином часу. Середнє значення на основі моделі та інші результати описового аналізу середньої річної частоти кровотеч, які потребували лікування, наведені в таблиці 2.
Таблиця 2. Середня річна частота кровотеч у разі профілактичного лікування препаратом Гімпавзі з плином часу в пацієнтів віком ≥ 12 років без вироблення інгібіторів фактора VIII або фактора IX
|
Значення |
Часовий інтервал |
||
|
Перші 6 місяців ФАЛ (N = 116) |
Другі 6 місяців ФАЛ (N = 112) |
B7841007* (N = 87) |
|
|
Кровотечі, які потребували лікування |
|||
|
Середнє значення ABR (95 % ДІ) |
4,95 (3,67; 6,68) |
3,25 (2,38; 4,42) |
2,79 (1,90; 4,09) |
|
Медіана ABR (IQR) |
2,00 (0,00; 5,99) |
1,91 (0,00; 4,09) |
0,00 (0,00; 4,10) |
* Пацієнти отримували марстацимаб протягом додаткового періоду до 16 місяців (у середньому 7 місяців) під час дослідження B7841007.
· Розрахункові середні значення та довірчі інтервали (ДІ) для середньої річної частоти кровотеч розраховані на базі моделі негативної біноміальної регресії.
· Медіана та міжквартильний діапазон (interquartile range (IQR)), від 25-го до 75-го процентилю, для середньої річної частоти кровотеч, отримані в результаті описового аналізу.
· ABR — середня річна частота кровотеч; ДІ — довірчий інтервал; IQR — міжквартильний розмах; ФАЛ — фаза активного лікування (B7841005); N — кількість пацієнтів, дані яких використовувалися для аналізу для кожного часового інтервалу.
Імуногенність
Протягом 12-місячного періоду лікування в ключовому дослідженні III фази B7841005 у 23 зі 116 (19,8 %) пацієнтів, які отримували лікування марстацимабом і у яких можна було оцінити рівень антитіл до препарату (ADA), вироблялися ADA. ADA були транзиторними у 61 % (14/23) та стійкими у 39 % (9/23) пацієнтів з наявністю ADA, що свідчить про транзиторний профіль ADA у більшості пацієнтів. До кінця дослідження титри ADA зникли у 22/23 (95,7 %) пацієнтів. Нейтралізуючі антитіла (NAb) виникли у 6 зі 116 (5,2 %) пацієнтів, які отримували лікування марстацимабом і у яких можна було оцінити рівень ADA, під час дослідження. NAb були транзиторними у всіх пацієнтів і жоден з них не мав NAb наприкінці дослідження. Хоча у пацієнтів з ADA спостерігалася трохи нижча концентрація марстацимабу (приблизно на 24–32 %) порівняно з пацієнтами без ADA, концентрація значною мірою збігалася у цих двох груп. Не виявлено клінічно значущого впливу ADA, включно з NAb, на безпеку або ефективність застосування марстацимабу протягом 12 місяців лікування. Загалом профіль безпеки марстацимабу був схожий у пацієнтів з ADA (включно з NAb) і без ADA.
У відкритому продовженні дослідження III фази тільки в одного із 44 пацієнтів, які продовжували отримувати марстацимаб протягом принаймні 6 місяців і в яких можна було оцінити рівень ADA, стабільно виявляли ADA.
Діти
Європейське агентство з лікарських засобів відтермінувало зобов’язання власника реєстраційного посвідчення надавати результати досліджень із застосуванням препарату Гімпавзі в одній або декількох підгрупах пацієнтів дитячого віку для лікування вродженої гемофілії A та вродженої гемофілії B.
Фармакокінетика
Фармакокінетику марстацимабу визначали за допомогою некомпартментного аналізу в здорових учасників та пацієнтів з гемофілією А і B, а також за допомогою популяційного фармакокінетичного аналізу бази даних, що складається з 213 учасників (150 пацієнтів із гемофілією та 63 здорових учасників), які отримували підшкірні (від 30 мг до 450 мг) або внутрішньовенні (150 і 440 мг) дози марстацимабу один раз на тиждень.
Марстацимаб продемонстрував нелінійну фармакокінетику системного впливу, який вимірювали за допомогою AUC і Cmax, що зростали швидше, ніж пропорційно дозі. Причинами цієї нелінійної фармакокінетики є цільовий розподіл препарату та залежне від концентрації нелінійне виведення марстацимабу, яке виникає, коли марстацимаб зв’язується з ендотеліальним інгібітором тканинного фактора.
Середній коефіцієнт накопичення в рівноважному стані для марстацимабу становив приблизно 3–4 відносно першої дози, після якої щотижнево застосовувалася доза 150 мг і 300 мг підшкірно. Очікується, що концентрації марстацимабу в рівноважному стані буде досягнуто приблизно через 60 днів, тобто на момент 8-ї або 9-ї підшкірної дози при застосуванні один раз на тиждень. Оцінка середніх показників Cmax,ss, Cmin,ss і Cavg,ss у популяції дорослих і дітей при щотижневому підшкірному застосуванні 150 мг марстацимабу наведена в таблиці 3.
Таблиця 3. Концентрація марстацимабу в плазмі крові в рівноважному стані після щотижневого підшкірного застосування 150 мг (з навантажувальною дозою 300 мг підшкірно)
|
Параметр |
Дорослі |
Діти |
|
Cmin,ss (нг/мл) |
13 700 (90,4 %) |
27 300 (53,2 %) |
|
Cmax,ss (нг/мл) |
17 900 (77,5 %) |
34 700 (48,5 %) |
|
Cavg,ss (нг/мл) |
16 500 (81,2 %) |
32 100 (49,5 %) |
· Дані наведені як арифметичні середні значення (%CV).
· Cmin,ss — мінімальна концентрація в плазмі в рівноважному стані; Cmax,ss — максимальна концентрація в плазмі в рівноважному стані; Cavg,ss — середня концентрація в плазмі в рівноважному стані.
Всмоктування
Після введення декількох підшкірних доз марстацимабу пацієнтам із гемофілією медіана Tmax становила від 23 до 59 годин. Оцінювана біодоступність марстацимабу після підшкірного застосування становила приблизно 71 % за результатами фармакокінетичного моделювання в популяції. Не спостерігалося релевантних відмінностей у біодоступності марстацимабу при введенні у руку, стегно і живіт.
Розподіл
Об’єм розподілу марстацимабу в рівноважному стані в пацієнтів із гемофілією становив 8,6 л на основі фармакокінетичного аналізу популяції. Цей обмежений позасудинний розподіл означає, що марстацимаб не виходить за межі внутрішньосудинного простору.
Біотрансформація
Дослідження метаболізму із застосуванням марстацимабу не проводилися. Очікується, що марстацимаб, подібно до інших терапевтичних білків з молекулярною масою вище за межу клубочкової фільтрації, піддається протеолітичному катаболізму та кліренсу, опосередкованому рецепторами. Крім того, на основі цільового розподілу препарату очікується, що марстацимаб також виводитиметься шляхом кліренсу, опосередкованого мішенню, через формування комплексу марстацимаб / інгібітор тканинного фактора.
Виведення
Дослідження виведення марстацимабу не проводилися. Зважаючи на молекулярну масу марстацимабу, очікується, що він піддається катаболічному розпаду і не виводиться нирками. Марстацимаб виводиться за допомогою лінійних і нелінійних механізмів. Після введення декількох підшкірних доз і на основі фармакокінетичного аналізу популяції лінійний кліренс марстацимабу становив приблизно 0,019 л/год. Середній ефективний період напіврозпаду марстацимабу в рівноважному стані становив приблизно від 16 до 18 днів як у дорослих, так і у дітей усіх груп за дозуванням.
Особливі групи пацієнтів
Маса тіла, вікова група, расова приналежність і тип гемофілії
Хоча маса тіла пацієнта була важливою коваріатою для опису фармакокінетики марстацимабу, немає потреби змінювати дозування через масу тіла для пацієнтів, маса тіла яких ≥ 35 кг. Кліренс марстацимабу (CL) був на 29 % нижчим у дітей (від 12 до < 18 років) порівняно з дорослими (віком від 18 років). Після коригування з урахуванням маси тіла кліренс (л/год/кг) у дітей, за оцінками, був приблизно на 3 % нижчим, ніж у дорослих, що вказує на те, що маса тіла є основним фактором відмінності кліренсу. Ця різниця фармакокінетики не призвела до клінічно значущої різниці в рівнях фармакодинамічного маркера пікового тромбіну між 2 групами на наступних етапах.
Не було виявлено клінічно значущого впливу типу гемофілії на фармакокінетику марстацимабу в популяції пацієнтів.
Расова приналежність (азійське чи інше походження) не була визначена як коваріата, яка впливає на фармакокінетику марстацимабу. У пацієнтів азійського походження кліренс марстацимабу з урахуванням маси тіла був на 32 % вищим, ніж у пацієнтів неазійського походження. Але така різниця не вважається клінічно значущою. Не існує достатньої кількості даних для оцінки потенційних відмінностей у впливі марстацимабу на людей іншої расової або етнічної приналежності.
Кількість учасників віком від 65 років у клінічних дослідженнях марстацимабу не була достатньою для оцінки різниці впливу марстацимабу порівняно з більш молодими пацієнтами.
Порушення функції нирок
Нирковий кліренс не вважається важливим для виведення моноклональних антитіл через їхній великий розмір і неефективну клубочкову фільтрацію. Клінічні дослідження впливу порушення функції нирок на фармакокінетику марстацимабу не проводилися.
Усі пацієнти з гемофілією A і B, включені в популяційний фармакокінетичний аналіз, мали нормальну функцію нирок (N = 129; eGFR ≥ 90 мл/хв/1,73 м2) або легке порушення функції нирок (N = 21; eGFR від 60 до 89 мл/хв/1,73 м2). Легке порушення функції нирок не вплинуло на фармакокінетику марстацимабу. Відсутні дані щодо застосування марстацимабу пацієнтам із порушенням функції нирок помірного або тяжкого ступеня.
Марстацимаб є моноклональним антитілом і виводиться за допомогою катаболізму, а не нирок, тому не передбачається необхідності зміни дози для пацієнтів із порушенням функції нирок.
Порушення функції печінки
Клінічні дослідження впливу порушення функції печінки на фармакокінетику марстацимабу не проводилися, оскільки таке порушення зазвичай не вважається значущим для моноклональних антитіл.
Усі пацієнти з гемофілією A і B, включені в клінічні дослідження, мали нормальну функцію печінки (N = 135; загальний білірубін і АСТ ≤ ВМН) або легке порушення функції печінки (N = 15; загальний білірубін від > 1× до ≤ 1,5× ВМН). Легке порушення функції печінки не вплинуло на фармакокінетику марстацимабу. Відсутні дані щодо застосування марстацимабу пацієнтам із порушенням функції печінки помірного або тяжкого ступеня.
Марстацимаб є моноклональним антитілом і виводиться за допомогою катаболізму, а не метаболізму в печінці, тому не передбачається необхідності зміни дози для пацієнтів із порушенням функції печінки.
Клінічні характеристики
Показання
Препарат Гімпавзі показаний для планової профілактики кровотеч у пацієнтів віком від 12 років та з масою тіла не менше 35 кг із такими захворюваннями:
· тяжка гемофілія А (вроджений дефіцит фактора VIII, FVIII < 1 %) без вироблення інгібіторів фактора VIII або
· тяжка гемофілія B (вроджений дефіцит фактора IX, FIX < 1 %) без вироблення інгібіторів фактора IX.
Протипоказання
Гіперчутливість до діючої речовини або будь-якої з допоміжних речовин препарату, зазначених у розділі «Склад».
Взаємодія з іншими лікарськими засобами та інші види взаємодій
Клінічні дослідження взаємодії марстацимабу з іншими лікарськими засобами не проводилися. Очікується, що як моноклональне антитіло марстацимаб виводитиметься шляхом катаболізму. Таким чином, вплив на його кліренс внаслідок взаємодії із супутніми лікарськими засобами, які виводяться некатаболічними шляхами, малоймовірний. Непрямий вплив таких біологічних препаратів, як марстацимаб, на експресію ферментів цитохрому P450 також не передбачається.
Особливості застосування
Простежуваність
Задля оптимізації простежуваності біологічних лікарських засобів потрібно точно вказувати в документації назву та номер серії препарату, який вводять.
Тромбоемболічні реакції
Припинення інгібування за допомогою інгібіторів тканинного фактора може збільшити потенціал зсідання крові пацієнта і стати одним із чинників індивідуального багатофакторного ризику виникнення тромбоемболічних реакцій у пацієнта. Підвищений ризик тромбоемболічних реакцій у разі застосування цього лікарського засобу може бути в пацієнтів:
· з ішемічною хворобою серця, венозним або артеріальним тромбозом або ішемічною хворобою в анамнезі;
· із гострим тяжким захворюванням із підвищеною експресією тканинного фактора (наприклад, серйозні інфекції, сепсис, травми, травми з роздавленням тканин, онкологічні захворювання).
Не вивчали застосування марстацимабу пацієнтам із тромбоемболічними реакціями в анамнезі (див. розділ «Фармакодинаміка»), а досвід застосування пацієнтам із гострими тяжкими захворюваннями обмежений.
Застосування інших інгібіторів тканинного фактора пов’язували з розвитком тромбоемболічних ускладнень у пацієнтів, які зазнали впливу додаткових гемостатичних засобів (наприклад препаратів обхідної дії) безпосередньо до чи після таких інгібіторів. Не спостерігалося жодного випадку тромбоемболічної реакції в пацієнтів із гемофілією, які отримували профілактичне лікування марстацимабом у межах клінічних досліджень. Препарати фактора VIII і фактора IX безпечно застосовували для лікування проривних кровотеч у пацієнтів, які отримують марстацимаб. Якщо пацієнту, який отримує профілактичне лікування препаратом Гімпавзі, показані препарати фактора VIII або фактора IX, рекомендовано застосовувати мінімальну ефективну дозу препарату згідно з інструкцією з медичного застосування.
Слід враховувати користь і ризик застосування препарату Гімпавзі для пацієнтів із тромбоемболічними реакціями в анамнезі або гострим тяжким захворюванням. Пацієнтам із підвищеним ризиком слід провести діагностику ранніх ознак тромбозу, а також застосувати профілактичні заходи проти тромбоемболії відповідно до поточних рекомендацій і стандарту лікування. Якщо результати діагностики свідчать про розвиток тромбоемболії, слід лікувати її за клінічними показаннями, а профілактичне лікування препаратом Гімпавзі – тимчасово припинити.
Рекомендації з лікування проривних кровотеч
Препарати фактора VIII і фактора IX можна застосовувати для лікування проривних кровотеч у пацієнтів, які отримують препарат Гімпавзі. Не слід застосовувати додаткові дози препарату Гімпавзі для лікування проривних кровотеч. Медичним працівникам слід за необхідності обговорювати з усіма пацієнтами та (або) особами, які доглядають їх, дозу та графік застосування концентратів фактора зсідання під час профілактичного лікування препаратом Гімпавзі, зокрема застосування мінімальної можливої ефективної дози концентрату фактора зсідання. Також слід ознайомитися з інформацією про застосовуваний концентрат фактора зсідання крові.
Реакції гіперчутливості
У пацієнтів, які отримували марстацимаб, розвивалися шкірні реакції у формі висипу і свербежу, які можуть свідчити про гіперчутливість до препарату (див. розділ «Побічні реакції»). Якщо у пацієнтів, які отримували лікування Гімпавзі, розвинулася тяжка реакція гіперчутливості, слід рекомендувати припинити застосування Гімпавзі та негайно звернутися за невідкладним лікуванням.
Пацієнт із виробленням інгібітора фактора
У межах поточного клінічного дослідження із застосуванням препарату не за затвердженими показаннями пацієнтам із гемофілією, в яких вироблялися інгібітори і які отримують лікування марстацимабом, в одного (2,9 %) пацієнта з тяжкою гемофілією B і алергічною реакцією на екзогенний фактор IX в анамнезі виник сильний висип приблизно через 9 місяців лікування. Пацієнту був необхідний тривалий курс пероральних кортикостероїдів, а лікування марстацимабом було припинено.
Вплив марстацимабу на результати коагуляційних проб
Лікування марстацимабом не призводить до клінічно значущих змін стандартних показників коагуляції, зокрема активованого часткового тромбопластинового часу і протромбінового часу.
Допоміжні речовини
Вміст полісорбату
Цей лікарський засіб містить полісорбат 80. Полісорбат 80 може викликати реакції гіперчутливості.
Вміст натрію
Цей лікарський засіб містить менше 1 ммоль (23 мг) натрію на 1 мл, тобто практично не містить натрію.
Застосування у період вагітності або годування груддю
Жінки репродуктивного віку
Жінкам репродуктивного віку, які отримують препарат Гімпавзі, слід застосовувати ефективну контрацепцію під час такого лікування та принаймні протягом 1 місяця після його припинення.
Вагітність
Клінічні дослідження застосування марстацимабу за участю вагітних жінок не проводилися. Дослідження репродуктивної функції у тварин під час застосування марстацимабу не проводилися. Невідомо, чи може препарат Гімпавзі завдати шкоди плоду при застосуванні вагітним жінкам або вплинути на репродуктивну функцію. Препарат Гімпавзі слід застосовувати в період вагітності, тільки якщо потенційна користь для вагітної переважує ризик для плода з урахуванням підвищення ризику тромбозу під час вагітності і після пологів, а також зв’язку декількох ускладнень вагітності з підвищеним ризиком синдрому дисемінованого внутрішньосудинного зсідання крові.
Годування груддю
Невідомо, чи потрапляє марстацимаб у грудне молоко людини. Дослідження впливу марстацимабу на вироблення молока або його вмісту в грудному молоці не проводилися. Відомо, що IgG людини виводиться з грудним молоком протягом перших декількох днів після пологів, але його концентрація швидко знижується; отже, не можна виключити ризик для немовляти на грудному вигодовуванні протягом цього короткого періоду. Після цього марстацимаб можна застосовувати під час грудного вигодовування у разі клінічної необхідності.
Репродуктивна функція
Результати досліджень на тваринах свідчать про відсутність прямого чи опосередкованого шкідливого впливу на репродуктивну функцію. Дані щодо впливу на репродуктивну функцію людини відсутні. Таким чином, вплив марстацимабу на чоловічу і жіночу репродуктивну функцію невідомий.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами
Препарат Гімпавзі не впливає або майже не впливає на здатність керувати транспортними засобами та працювати з іншими механізмами.
Спосіб застосування та дози
Лікування слід розпочинати під наглядом медичного працівника, який має досвід лікування гемофілії. Лікування слід починати за умови відсутності кровотечі в пацієнта.
Дози
Рекомендована доза для пацієнтів віком від 12 років та з масою тіла не менше 35 кг становить 300 мг як початкова навантажувальна доза, яку вводять шляхом підшкірної ін’єкції, і далі – 150 мг шляхом підшкірної ін’єкції один раз на тиждень у будь-який час доби.
Тривалість лікування
Препарат Гімпавзі призначений для довгострокового профілактичного лікування.
Корекція дози під час терапії
Можна розглянути необхідність скоригувати дозу до 300 мг шляхом підшкірної ін’єкції щотижня для пацієнтів з масою тіла ≥ 50 кг, якщо медичний працівник вважає, що забезпечується недостатній рівень зупинки кровотеч. Максимальна тижнева доза не повинна перевищувати 300 мг.
Рекомендації з лікування проривних кровотеч
Не слід застосовувати додаткові дози препарату Гімпавзі для лікування проривних кровотеч. Див. рекомендації з лікування проривних кровотеч у розділі «Особливості застосування».
Лікування пацієнтів із гострим тяжким захворюванням
При гострих тяжких захворюваннях із підвищеною експресією тканинного фактора, як-от інфекція, сепсис і травми з роздавленням тканин, потенціювання запальної реакції за допомогою одночасного застосування інгібітора тканинного фактора може становити ризик побічних реакцій, зокрема тромбозу (див. розділ «Особливості застосування»).
Гострі тяжкі захворювання слід лікувати відповідно до місцевого стандарту лікування, а необхідність подальшого лікування препаратом Гімпавзі у цій ситуації слід розглянути з урахуванням потенційних ризиків. При застосуванні марстацимабу для цих пацієнтів може бути потрібний додатковий моніторинг побічних реакцій і розвитку тромбоемболії. Слід тимчасово припинити застосування препарату Гімпавзі, якщо клінічні симптоми, результати візуалізаційних та (або) лабораторних досліджень свідчать про виникнення тромботичних реакцій. Ці реакції слід лікувати за клінічними показаннями. Лікування препаратом Гімпавзі можна поновити після клінічного одужання пацієнта згідно з клінічним висновком медичного працівника (див. «Пропуск дози» нижче).
Пропуск дози
У разі пропуску дози препарат вводять якомога швидше до дня наступної запланованої дози, а потім поновлюють звичайний щотижневий графік застосування.
Якщо через пропуск дози пройшло більше 13 днів після останньої дози, слід ввести навантажувальну дозу 300 мг шляхом підшкірної ін’єкції, а потім повернутися до застосування 150 мг шляхом підшкірної ін’єкції один раз на тиждень.
Перехід на препарат Гімпавзі
Перехід від профілактичної замісної терапії факторами зсідання крові на застосування препарату Гімпавзі: до початку лікування препаратом Гімпавзі пацієнтам слід припинити лікування концентратами факторів зсідання крові (концентратами фактора VIII або фактора IX). Можна почати лікування препаратом Гімпавзі в будь-який час після припинення застосування концентратів факторів зсідання.
Перехід від застосування нефакторних лікарських засобів для лікування гемофілії на застосування препарату Гімпавзі: відсутні дані клінічних досліджень, на підставі яких можна надати рекомендації щодо переведення пацієнтів з лікування нефакторними лікарськими засобами на застосування марстацимабу. Хоча період вимивання не вивчався, один з можливих підходів — забезпечити достатній період вимивання попереднього препарату (принаймні 5 періодів напіввиведення) на основі зазначеного на етикетці періоду напіввиведення до початку лікування препаратом Гімпавзі. Під час переходу із застосування інших нефакторних лікарських засобів від гемофілії до застосування препарату Гімпавзі може бути потрібна гемостатична підтримка за допомогою концентратів факторів зсідання крові.
Особливі групи пацієнтів
Порушення функції печінки
Для пацієнтів із легким або помірним порушенням функції печінки корекція дози не рекомендується (див. розділ «Фармакокінетика»). Застосування марстацимабу пацієнтам з порушенням функції печінки помірного або тяжкого ступеня не досліджувалося.
Порушення функції нирок
Для пацієнтів із легким або помірним порушенням функції нирок корекція дози не рекомендується (див. розділ «Фармакокінетика»). Застосування марстацимабу пацієнтам з порушенням функції нирок помірного або тяжкого ступеня не досліджувалося.
Пацієнти літнього віку
Для пацієнтів віком понад 65 років корекція дози не рекомендується (див. розділ «Фармакокінетика»).
Застосування в періопераційний період
Безпека та ефективність застосування марстацимабу в хірургії не оцінювалися формально. У межах клінічних досліджень пацієнти проходили незначні хірургічні процедури без припинення профілактичного лікування із застосуванням препарату Гімпавзі.
У разі проведення серйозних хірургічних втручань рекомендовано припинити застосування препарату Гімпавзі за 6–12 днів до операції та почати лікування за місцевим стандартом із застосуванням концентратів фактора зсідання крові і заходів для зменшення ризику венозного тромбозу, який може бути підвищеним у періопераційний період. Ознайомтеся з інформацією про лікарський засіб для концентрату фактора зсідання, в якій наведені рекомендацій щодо дозування для пацієнтів із гемофілією, які переносять серйозне хірургічне втручання. При поновленні застосування препарату Гімпавзі слід враховувати загальний клінічний стан пацієнта, включно з наявністю факторів ризику тромбоемболії після хірургічного втручання, застосування інших гемостатичних засобів та інших супутніх лікарських засобів (див. розділ «Пропуск дози» вище).
Спосіб застосування
Препарат Гімпавзі призначений виключно для підшкірного застосування.
Препарат Гімпавзі призначений для застосування під наглядом медичного працівника. Після належного навчання техніки виконання підшкірних ін’єкцій лікарський засіб може вводити пацієнт або особа, яка за ним доглядає, якщо медичний працівник вирішить, що це доречно.
Перед підшкірним застосуванням препарат Гімпавзі можна вийняти з холодильника і залишити за кімнатної температури в коробці на 15–30 хвилин подалі від прямих сонячних променів (див. розділи «Умови зберігання»). Лікарський засіб не слід підігрівати за допомогою джерела тепла, як-от гаряча вода або мікрохвильова піч.
Рекомендовано робити ін’єкції у живіт і стегно. За необхідності можливе використання інших місць. Вводити препарат Гімпавзі у сідниці (тільки з попередньо наповненої ручки) має виключно особа, яка доглядає за пацієнтом, або медичний працівник. Лікарський засіб не слід вводити поблизу кісток або ділянки шкіри, де є синці, почервоніння, болючість (чутливість) або ущільнення, а також ділянки зі шрамами чи розтяжками.
Дві ін’єкції по 150 мг препарату Гімпавзі, які застосовуються як навантажувальна доза 300 мг, слід виконувати в різні місцях.
Рекомендується змінювати місце ін’єкції по колу для кожного введення.
Не слід вводити препарат Гімпавзі у вену або м’яз.
Під час лікування препаратом Гімпавзі бажано вводити інші лікарські засоби для підшкірного застосування в різні ділянки тіла.
Інформація для пацієнта
Інструкція щодо застосування попередньо наповненої ручки для ін’єкцій
|
Ковпачок голки |
|
Голка (усередині запобіжника голки) |
|
Жовта смужка у віконці |
|
Закритий запобіжник голки |
|
Шток шприца |
|
Попередньо наповнена ручка з препаратом Гімпавзі ПІСЛЯ застосування |
|
Дозування |
|
Дата терміну придатності |
|
Віконце |
|
Відкритий запобіжник голки |
|
Кришка |
|
Попередньо наповнена ручка з препаратом Гімпавзі ПЕРЕД застосуванням |
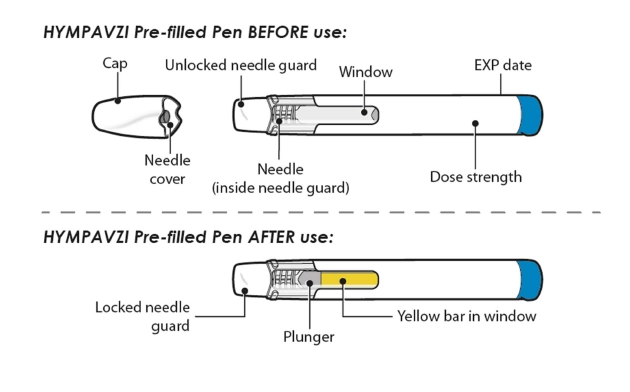
Зовнішній вигляд ручки може відрізнятися.
Етапи підготовки
Етап 1
Підготовка
Вилучіть ручку з коробки та тримайте її подалі від прямих сонячних променів.
· Переконайтеся, що назва препарату Гімпавзі зазначена на коробці та етикетці ручки.
· Перевірте ручку щодо видимих пошкоджень, як-от тріщини або протікання.
· Вимийте і висушіть руки.
· Не знімайте ковпачок, доки не будете готові до ін’єкції.
· Утилізуйте ручку у випадку пошкодження або падіння ручки чи коробки з нею.
· Заборонено застосовувати ручку в таких випадках:
o Якщо вона зберігалася під прямими сонячними променями. Вплив кімнатного світла під час підготовки дози та ін’єкції є прийнятним.
o Ручка була заморожена, розморожена або вилучена з холодильника більше ніж 7 днів тому.
· Не струшуйте ручку. Струшування може зашкодити препарату Гімпавзі.
Примітка. Для комфортнішого введення залиште ручку при кімнатній температурі в коробці подалі від прямих сонячних променів приблизно на 15–30 хвилин.
Заборонено застосовувати будь-які інші методи для підігрівання ручки, як-от нагрівання в мікрохвильовій печі або гарячій воді.
Етап 2
Перевірте термін придатності
· Перевірте термін придатності, надрукований на етикетці ручки.
· Не застосовуйте її, якщо сплив термін придатності.
|
Етап 3 |
|
Перевірте препарат |
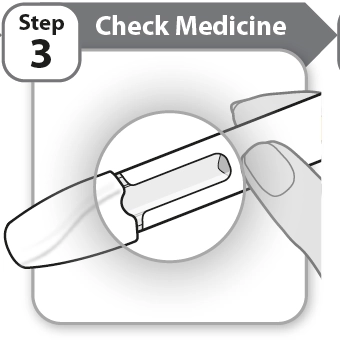
· Уважно огляньте препарат через віконце на ручці.
o Препарат має бути прозорим, безбарвним або світло-жовтого кольору.
o Не застосовуйте ручку, якщо препарат каламутний, темно-жовтого кольору або містить пластівці чи частинки.
Примітка. У віконці можна побачити бульбашки повітря. Це нормально.
Якщо у вас виникли запитання щодо препарату, зверніться до лікаря або медсестри.
|
Етап 4 |
|
Виберіть і підготуйте місце ін’єкції |
|
Ділянка живота (черевна стінка) |
|
Стегно |
|
Сідниці |
|
Вводити препарат може тільки лікар, медсестра чи особа, яка доглядає за пацієнтом |
|
Тримайте ручку в радіусі не менше 5 см навколо пупка |
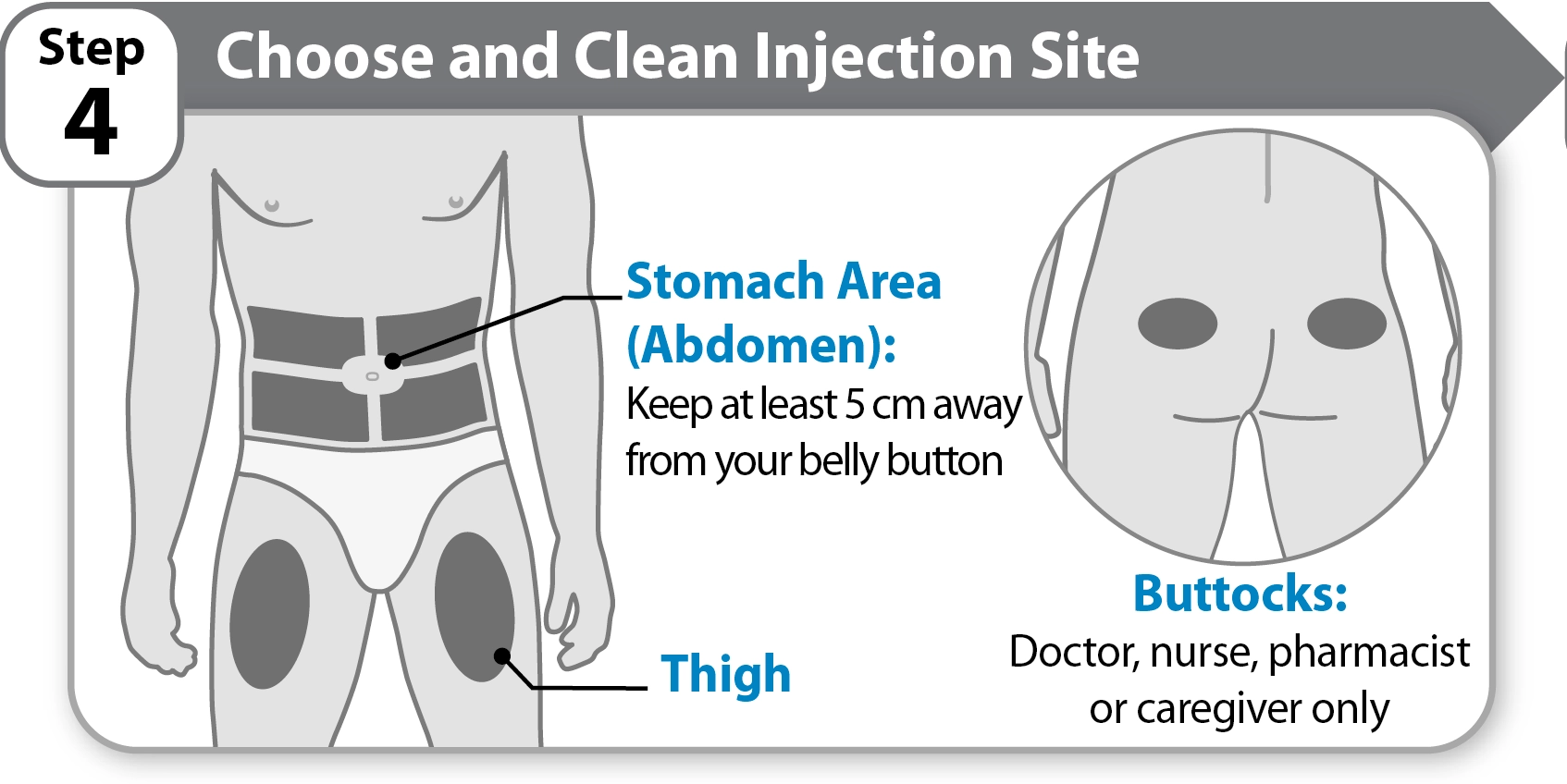
· Виберіть місце ін’єкції на ділянці живота (черевної стінки) або стегна, якщо лікар чи медсестра не пропонують інше місце. Препарат Гімпавзі також можна вводити в сідниці (тільки лікар, медсестра або особа, яка доглядає за пацієнтом). Тримайте ручку в радіусі не менше 5 см навколо пупка.
· Змінюйте місце ін’єкції щоразу, коли вводите препарат Гімпавзі самостійно. Можна вводити препарат в одну й ту саму ділянку тіла, але обов’язково вибирайте інше місце для ін’єкції.
· Помийте місце ін’єкції водою з милом або очистьте спиртовою серветкою, якщо це зручно.
· Зачекайте, доки ділянка висохне. Не торкайтеся очищеного місця ін’єкції, не сушіть його вентилятором і не дуйте на нього.
· Не вводьте препарат Гімпавзі в кісткові ділянки або ділянки шкіри, де є синці, почервоніння, болючість (чутливість) чи ущільнення. Уникайте ділянок зі шрамами або розтяжками.
· Не можна вводити препарат Гімпавзі у вену або м’яз.
· Не вводьте препарат Гімпавзі через одяг.
|
Етап 5 |
|
Відкрутіть кришку |
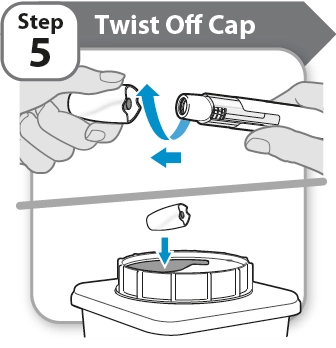
· Поверніть і зніміть кришку.
· Відразу покладіть кришку в контейнер для використаних гострих предметів. Вона більше не знадобиться.
Примітка.
o Ви можете побачити кілька крапель препарату на кінці голки. Це нормально.
o Після зняття кришки ковпачок голки залишається всередині кришки.
Обережно! Необхідно обережно поводитися з ручкою, оскільки вона містить голку.
Не кладіть і не тисніть рукою на запобіжник голки. Це може призвести до пошкодження голки.
Етапи введення препарату
|
Введіть препарат |
|
Щільно притисніть до шкіри |
|
Продовжуйте притискати |
|
Порахуйте |
|
Етап 6 |
|
Перше клацання |
|
Друге клацання |
|
1…2…3…4…5 |
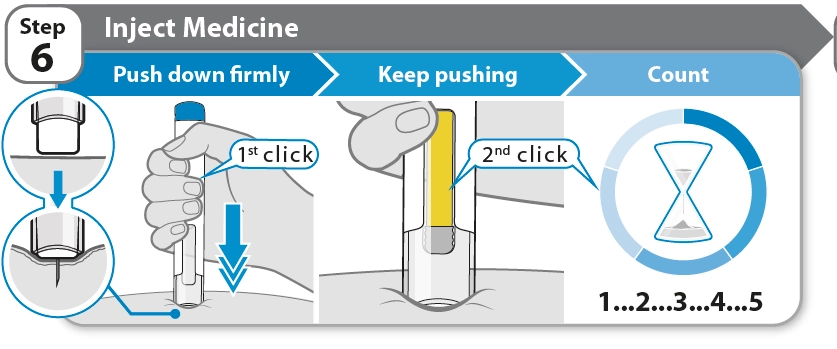
· Щільно притисніть ручку до шкіри під кутом 90° і продовжуйте притискати до завершення ін’єкції (див. етап 7). Коли ін’єкція розпочнеться, ви почуєте перше клацання.
· Продовжуйте притискати ручку щільно до шкіри, поки жовта смужка рухається вздовж віконця. Ви почуєте друге клацання, коли ін’єкція майже завершена.
· Почувши друге клацання, повільно порахуйте до п’яти, щоб переконатися, що ви ввели повну дозу.
Не прибирайте ручку, поки не дорахуєте повільно до п’яти після другого клацання, а жовтий маркер повністю не заповнить віконце.
Примітка. При натисканні на ручку голка входить у шкіру. Лікар або медсестра може порадити м’яко защипнути шкіру під час ін’єкції.
Примітка. Якщо ви не чуєте клацання під час натискання ручки на шкіру, спробуйте натиснути донизу сильніше. Якщо ін’єкція так і не почалася, візьміть нову попередньо наповнену ручку з препаратом Гімпавзі.
Обережно! Якщо ви вирішили зробити ін’єкцію в інше місце після введення голки в шкіру, потрібно утилізувати цю ручку і скористатися новою попередньо наповненою ручкою із препаратом Гімпавзі.
|
Етап 7 |
|
Приберіть ручку |
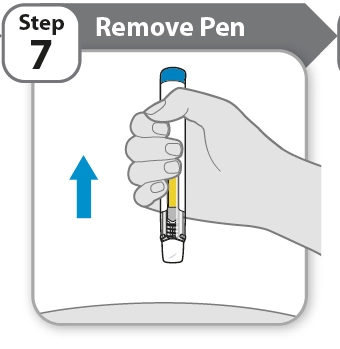
· Приберіть ручку від шкіри.
o Якщо на шкірі залишилася невелика крапля препарату, під час наступної ін’єкції почекайте трохи довше перед вилученням ручки.
Примітка. Після прибирання ручки від шкіри голка автоматично покривається ковпачком, а запобіжник голки блокується на місці.
Заборонено використовувати ручку повторно.
|
Етап 8 |
|
Перевірте віконце |
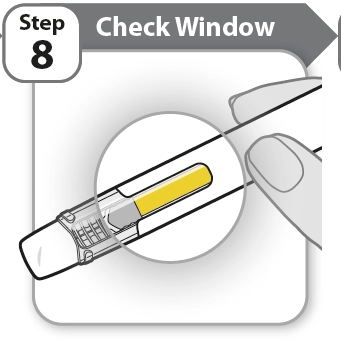
· Перевірте віконце та переконайтеся, що лікарський засіб введено повністю.
Якщо жовта смужка не перебуває в показаному положенні, ви не ввели повну дозу. Зверніться до лікаря або медсестри по допомогу.
Не вводьте додаткову дозу.
|
Етап 9 |
|
Після ін’єкції |
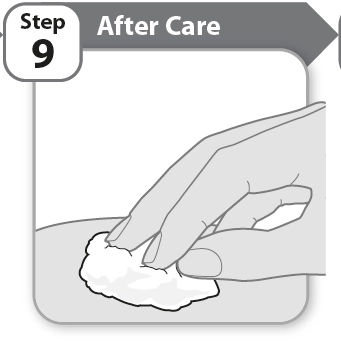
· Злегка притисніть місце ін’єкції чистим ватним або марлевим тампоном на декілька секунд, якщо з’явилася крапля крові.
· Не можна терти місце ін’єкції.
Примітка. Якщо кровотеча не припиняється, зверніться до лікаря або медсестри.
|
Етап 10 |
|
Утилізуйте використану ручку |
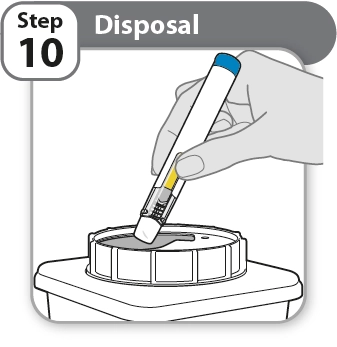
· Покладіть використану ручку в контейнер для використаних гострих предметів згідно з інструкціями лікаря або медсестри, а також місцевими законами про охорону здоров’я та безпеку.
· Не викидайте (не утилізуйте) ручки із побутовим сміттям.
Діти
Препарат Гімпавзі не слід застосовувати дітям віком до 1 року через потенційні проблеми з безпекою. Безпека та ефективність застосування марстацимабу дітям віком до 12 років дотепер не встановлені. Безпека та ефективність застосування марстацимабу дітям з масою тіла менше 35 кг не встановлені. Дані відсутні.
Передозування
Існує обмежений досвід передозування марстацимабу.
Не спостерігалося серйозних побічних реакцій у невеликої кількості дорослих пацієнтів з масою тіла ≥ 50 кг, які отримували марстацимаб у дозі 450 мг щотижня шляхом підшкірного застосування протягом періоду до 3 місяців під час досліджень попередніх фаз. Однак це була невелика група, тому ефект довгострокового впливу у високій дозі невідомий. Застосування доз, вищих за рекомендовані, може призвести до гіперкоагуляції.
Пацієнтам, які зазнали випадкового передозування, слід негайно звернутися до медичного працівника для уважного спостереження. У разі передозування рекомендовано негайно встановити спостереження за станом пацієнта для виявлення будь-яких ознак або симптомів побічних реакцій та (або) гіперкоагуляції та провести відповідне симптоматичне лікування.
Діти
Застосування доз понад 150 мг на тиждень у дітей віком від 12 до 17 років включно з масою тіла < 50 кг не вивчалося. У дітей не було зареєстровано жодного випадку передозування. Принципи, описані вище, застосовуються до лікування передозування в дітей.
Побічні реакції
Загальна інформація щодо профілю безпеки
Найчастіше повідомлялося про розвиток реакцій у місці ін’єкції (11,2 %) після лікування марстацимабом.
Список побічних реакцій у формі таблиці
Дані з безпеки в таблиці 4 базуються на об’єднаних даних з дослідження безпеки та ефективності III фази (BASIS) та його відкритого продовження (див. розділ «Фармакодинаміка»). Дані 12‑місячного періоду активного лікування в межах ключового дослідження III фази відображають вплив застосування марстацимабу один раз на тиждень на 116 пацієнтів чоловічої статі з гемофілією A або B, у яких не вироблялися інгібітори. Дев’яносто сім (83,6 %) пацієнтів були дорослими (віком від 18 років), а 19 (16,4 %) — дитячого віку (від 12 до 18 років). На момент припинення збору даних всього 87 зі 116 пацієнтів, які закінчили 12-місячний період лікування, були включені до відкритого продовження дослідження. Медіанна тривалість застосування становила 518,5 дня (від 28 до 847 днів).
У таблиці 4 узагальнено побічні реакції, що спостерігалися в пацієнтів, які отримували профілактичне лікування марстацимабом. Побічні реакції, зазначені в таблиці 4, класифіковані за системно-органним класом (СОК) і такими загальноприйнятими категоріями частоти виникнення: дуже часто (≥ 1/10), часто (від ≥ 1/100 до < 1/10), нечасто (від ≥ 1/1000 до < 1/100), рідко (від ≥ 1/10 000 до < 1/1000), дуже рідко (< 1/10 000) або частота невідома (не можна оцінити за наявними даними). У кожній групі частоти побічні реакції зазначені в порядку зниження їхньої серйозності.
Таблиця 4. Побічні реакції
|
Системно-органний клас |
Побічна реакція |
Частота |
|
Порушення з боку нервової системи |
Головний біль |
Часто |
|
Порушення з боку судин |
Артеріальна гіпертензія |
Часто |
|
Порушення з боку шкіри та підшкірної клітковини |
Висип Свербіж |
Нечасто Часто |
|
Загальні розлади та реакції в місці введення |
Реакції в місці введенняа |
Дуже часто |
а Див. «Опис окремих побічних реакцій».
Опис окремих побічних реакцій
Реакції у місці введення
Загалом 11,2 % пацієнтів, які отримували марстацимаб, повідомили про розвиток реакцій в місці введення. Більшість реакцій в місці введення, які спостерігалися в клінічних дослідженнях марстацимабу, були тимчасовими і мали легкий або помірний ступінь тяжкості. Жодна реакція в місці введення не потребувала коригування дози або припинення застосування препарату. Реакції в місці введення включають синці в місці ін’єкції, еритему в місці ін’єкції, гематоми в місці ін’єкції, ущільнення в місці ін’єкції, набряк у місці ін’єкції, біль у місці ін’єкції і свербіж у місці ін’єкції.
Висип
У популяції пацієнтів, в яких не вироблялися інгібітори, 0,9 % пацієнтів повідомили про несерйозні висипи (1 ступінь).
Діти
До популяції дітей у дослідженні входило 19 пацієнтів дитячого віку (від 12 до < 18 років). Профіль безпеки марстацимабу був загалом однаковий у дітей і дорослих.
Повідомлення про підозрювані побічні реакції
Повідомлення про побічні реакції після реєстрації лікарського засобу має важливе значення. Це дає змогу проводити моніторинг співвідношення користь/ризик при застосуванні цього лікарського засобу. Медичним та фармацевтичним працівникам, а також пацієнтам або їхнім законним представникам слід повідомляти про усі випадки підозрюваних побічних реакцій та відсутності ефективності лікарського засобу через Автоматизовану інформаційну систему з фармаконагляду за посиланням: https://aisf.dec.gov.ua
Несумісність
У зв’язку з тим, що дослідження сумісності цього лікарського засобу не проводилися, його не можна змішувати з іншими лікарськими засобами.
Термін придатності. 3 роки.
Умови зберігання
Зберігати в недоступному для дітей місці.
Зберігати в холодильнику (2–8 °C) в оригінальній картонній коробці для захисту від світла. Не заморожувати.
Цей лікарський засіб можна виймати з холодильника, в якому він зберігається, і зберігати в оригінальній картонній коробці протягом єдиного періоду, що становить максимум 7 днів, за кімнатної температури не вище 30 °C. Лікарський засіб не слід повертати на зберігання до холодильника. До кінця цього періоду зберігання за кімнатної температури лікарський засіб необхідно застосувати або утилізувати.
Упаковка
По 1 попередньо наповненій ручці, що містить шприц, у картонній коробці з маркуванням українською та англійською мовами.
Категорія відпуску. за рецептом.
Виробник
Пфайзер Менюфекчуринг Бельгія НВ.
Місцезнаходження виробника та адреса місця провадження його діяльності
Рейксвег 12, Пуурс-Сінт-Амандс, 2870, Бельгія.
